
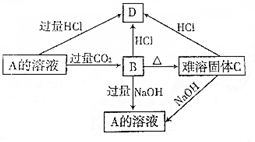
分析 A、B、C、D是中学化学中常见的四种化合物,它们之间有如图所示的转化关系;取溶液A灼烧,火焰呈黄色,说明A中含有Na元素,A的溶液能和过量CO2反应生成B,B是一种白色难溶物,B能和HCl、NaOH溶液反应,则B是Al(OH)3,A为NaAlO2,D为AlCl3,B加热分解生成难溶性固体C,C能和NaOH溶液反应生成NaAlO2,则C是Al2O3,据此分析解答.
解答 解:A、B、C、D是中学化学中常见的四种化合物,它们之间有如图所示的转化关系;取溶液A灼烧,火焰呈黄色,说明A中含有Na元素,A的溶液能和过量CO2反应生成B,B是一种白色难溶物,B能和HCl、NaOH溶液反应,则B是Al(OH)3,A为NaAlO2,D为AlCl3,B加热分解生成难溶性固体C,C能和NaOH溶液反应生成NaAlO2,则C是Al2O3,A→B、A→D、B→D、B→A、B→C、C→D、C→A反应方程式分别为NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3、NaAlO2+4HCl=NaCl+AlCl3+2H2O、Al(OH)3+3HCl=AlCl3+3H2O、Al(OH)3+NaOH=NaAlO2+2H2O、2Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3H2O、Al2O3+2NaOH=2NaAlO2+H2O、Al2O3+6HCl=2AlCl3+3H2O,
通过以上分析知,A、C分别是NaAlO2、Al2O3,
故答案为:NaAlO2;Al2O3.
点评 本题以Al及其化合物之间的转化为载体考查无机物推断,为高频考点,明确铝的化合物性质是解本题关键,知道氧化铝、氢氧化铝的两性,难点是偏铝酸钠和二氧化碳反应方程式的书写,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | Cu(OH)2+HCl;Cu(OH)2+CH3COOH | B. | NaHSO4+NaOH;H2SO4+NaOH | ||
| C. | NaHCO3+H2SO4;Na2CO3+HCl | D. | BaCl2与Na2SO4;Ba(OH)2与CuSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | V(A)=0.15mol/(l•s) | B. | V(B)=0.6mol/(l•s) | C. | V(C)=0.45mol/(l•s) | D. | V(D)=4.0mol/(l•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
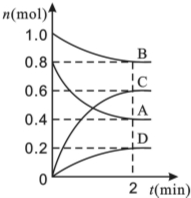 T℃时,在容积为0.5L的密闭容器中发生某一反应,且测得不同时间容器中四种物质A、B、C、D的物质的量变化如图所示,已知:物质A、B、C均为气态,D为固态,正反应时吸热反应,根据要求回答下列问题:
T℃时,在容积为0.5L的密闭容器中发生某一反应,且测得不同时间容器中四种物质A、B、C、D的物质的量变化如图所示,已知:物质A、B、C均为气态,D为固态,正反应时吸热反应,根据要求回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 已知短周期元素A、B、C、D最高价氧化物对应水化物分别为X、Y、Z、W.A是短周期中原子半径最大的元素.常温下X、Z,W均可与Y反应,A、C、D的原子序数及0.1 mol/LX、Z、W溶液的pH如图所示.下列说法正确的是( )
已知短周期元素A、B、C、D最高价氧化物对应水化物分别为X、Y、Z、W.A是短周期中原子半径最大的元素.常温下X、Z,W均可与Y反应,A、C、D的原子序数及0.1 mol/LX、Z、W溶液的pH如图所示.下列说法正确的是( )| A. | B和D形成的化合物和W具有相同的化学键类型与晶体类型 | |
| B. | C氢化物稳定性大于D氢化物稳定性,而其水溶液的酸性D大于C | |
| C. | B与C所形成的化合物既可以由B、C的单质相互反应制得,也可由含B、C元素简单离子的盐溶液相互反应制得 | |
| D. | A、B、C、D四种元素均在第三周期,而其原子半径依次增大,对应简单离子的半径依次减小 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高二上第三次月考化学卷(解析版) 题型:选择题
反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g)在2L的密闭容器中进行,1min后,NH3减少了0.12mol,则平均每秒钟浓度变化正确的是
A.NO:0.06mol•L﹣1  B.H2O:0.002mol•L﹣1
B.H2O:0.002mol•L﹣1
C.NH3:0.002mol•L﹣1 D.O2:0.00125mol•L﹣1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高二上第一次月考化学卷(解析版) 题型:选择题
已知反应①:CO(g)+CuO(s) CO2(g)+Cu(s)和反应②:H2(g)+CuO(s)
CO2(g)+Cu(s)和反应②:H2(g)+CuO(s) Cu(s)+H2O(g)在相同的温度下的平衡常数分别为K1和K2,该温度下反应③:CO(g)+H2O(g)
Cu(s)+H2O(g)在相同的温度下的平衡常数分别为K1和K2,该温度下反应③:CO(g)+H2O(g) CO2(g)+H2(g)的平衡常数为K.则下列说法正确的是
CO2(g)+H2(g)的平衡常数为K.则下列说法正确的是
A.反应①的平衡常数K1=[c(C O2)•c(Cu)]/[c(CO)•c(CuO)]
O2)•c(Cu)]/[c(CO)•c(CuO)]
B.对于反应③,恒容时,温度升高,H2的浓度减小,则该反应的焓变为正值
C.反应③的平衡常数K=K1/K2
D.对于反应③,恒温恒容下,增大压强,H2的浓度一定减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com