
分析 某元素基态原子3P能级有一个单电子,根据能量最低原理,基态原子核外电子排布为:1s22s22p63s23p1或1s22s22p63s23p5;3p能级上有一个空轨道,根据能量最低原理,基态原子核外电子排布为:1s22s22p63s23p2;3P能级有一对孤对电子,根据能量最低原理,基态原子核外电子排布为:1s22s22p63s23p4,据此判断.
解答 解:某元素基态原子3P能级有一个单电子,根据能量最低原理,基态原子核外电子排布为:1s22s22p63s23p1或1s22s22p63s23p5,则该元素为Al或Cl;3p能级上有一个空轨道,根据能量最低原理,基态原子核外电子排布为:1s22s22p63s23p2,则该元素为Si;3P能级有一对孤对电子,根据能量最低原理,基态原子核外电子排布为:1s22s22p63s23p4,则该元素为S;
故答案为:Al或Cl;Si;S.
点评 本题考查核外电子排布,比较基础,注意掌握核外电子排布规律.


科目:高中化学 来源: 题型:选择题
| A. | 101 | B. | 258 | C. | 157 | D. | 359 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,W的最高正价为+7.
,W的最高正价为+7.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
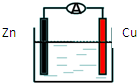
| A. | 锌做负极发生氧化反应 | |
| B. | 供电时的总反应为:Zn+2H+=Zn2++H2↑ | |
| C. | 该装置可实现化学能转化为电能 | |
| D. | 溶液中硫酸根离子向Cu极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 升高温度,H2S浓度增加,表明该反应是放热反应 | |
| B. | 通入CO后,正反应速率逐渐增大 | |
| C. | 反应前H2S物质的量为7mol | |
| D. | CO的平衡转化率为80% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应属于置换反应 | B. | CO作还原剂 | ||
| C. | Fe2O3发生氧化反应 | D. | CO被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素代号 | L | M | Q | R | T |
| 原子半径/nmm | 0.160 | 0.134 | 0.089 | 0.102 | 0.074 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A. | L2+与R2-的核外电子数相等 | B. | L与T形成的化合物具有两性 | ||
| C. | L和Q金属性:Q<L | D. | 氢化物的稳定性为H2T<H2R |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子或离子间相互的吸引力叫化学键 | |
| B. | 共价化合物可能含离子键,离子化合物中只含离子键 | |
| C. | 构成单质分子的微粒一定含有共价键 | |
| D. | 共价化合物内部可能有极性键和非极性键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com