
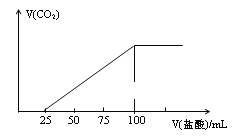
【题目】向100mLNaOH溶液中通入一定量的CO2气体,充分反应后,再向所得溶液中逐滴加入0.2mol·L-1的盐酸,产生CO2气体的体积与所加盐酸体积之间的关系如图所示。下列判断正确的是
A.所得溶液溶质成分的物质的量之比为:n(NaHCO3):n(Na2CO3)=2: 1
B.所得溶液溶质成分的物质的量之比为:(NaOH):n(Na2CO3)=1: 3
C.原NaOH溶液的浓度为0.1mol/L
D.通入CO2体积为448mL
【答案】A
【解析】
本题主要考查关于NaOH与CO2反应的计算。有关反应:Na2CO3+HCl=NaCl+NaHCO3,NaHCO3+HCl=NaCl+H2O+CO2↑。
A.由图象可知,混合物为碳酸钠和碳酸氢钠,混合物中滴加盐酸,由碳酸钠转化为碳酸氢钠,消耗25mL盐酸,则原有碳酸氢钠消耗100mL-25×2mL=50mL盐酸,所得溶液的溶质成分的物质的量之比为n(NaHCO3):n(Na2CO3)=50mL:25mL=2:1,故A正确;
B.根据A项分析,所得溶液的溶质成分为碳酸钠和碳酸氢钠,不含氢氧化钠,故B错误;
C.在加入100mL稀盐酸时,恰好生成氯化钠溶液,由原子守恒可知,原NaOH溶液的浓度为c=![]() =0.2mol/L,故C错误;
=0.2mol/L,故C错误;
D.温度和压强不确定,通入CO2的体积也无法确定,故D错误。
答案:A。


科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、M为短周期主族元素。25℃时,其最高价氧化物对应的水化物(浓度均为0.01mol·L-1)溶液的pH和原子半径的关系如图所示。下列有关说法不正确的是( )
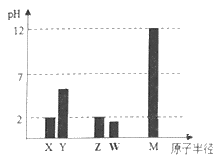
A.最简单气态氢化物的热稳定性:Z>W
B.Y的最高价氧化物的电子式为:![]()
C.W的气态氢化物是强酸
D.X、M两种元素形成的简单离子半径大小顺序:X>M
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A.氯气通入水中,溶液呈酸性:Cl2 + H2O ![]() 2H+ + Cl- + ClO-
2H+ + Cl- + ClO-
B.硅酸钠溶液与盐酸混合产生浑浊:SiO32-+2H+=H2SiO3↓
C.向FeBr2溶液中通入少量Cl2:Cl2 +2Br- = 2Cl-+ Br2
D.将磁性氧化铁溶于氢碘酸:Fe3O4+8H+=2Fe3++ Fe2++4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物J是治疗心脏病药物的一种中间体,分子结构中含有3个六元环。合成路线如图:
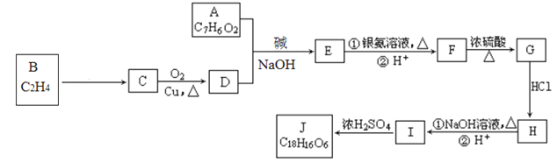
已知:R1—CHO+ R2—CH2—CHO![]()
![]() 。
。
请回答:
(1)已知:A能发生银镜反应,与![]() 溶液发生显色反应,核磁共振氢谱显示有4组峰,峰面积之比为1:2:2:1,则A的结构简式是__。
溶液发生显色反应,核磁共振氢谱显示有4组峰,峰面积之比为1:2:2:1,则A的结构简式是__。
(2)J的结构简式是__,G所含官能团的名称是__。
(3)写出A与D反应生成E的化学方程式__,H→I的反应类型是__。
(4)符合下列条件E的酸化产物的同分异构体有__种。
①苯环上有2个取代基②能遇FeCl3溶液发生显色反应③能发生水解反应
(5)结合题中给信息,设计以C2H4为原料反应制备1,3-丁二烯的合成路线___(其他试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机一无机活性材料的液流电池具有能量密度大、环境友好等特点。其负极反应为Zn-2e-+4NH3·H2O=Zn(NH3)42++4H2O,以LiPF6为电解质,工作示意图如图。电池放电过程中,下列说法错误的是
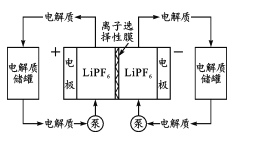
A.电子从负极经外电路流向正极
B.已知正极发生反应: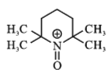 +e-→
+e-→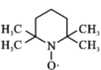 ,此过程为还原反应
,此过程为还原反应
C.负极附近溶液pH会降低
D.电解质溶液中的Li+自左向右移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛(Ti)被称为“未来金属”,广泛应用于国防、航空航天、生物材料等领域。钛的氯化物有如下转变关系:2TiCl3![]() TiCl4↑+TiCl2回答下列问题。
TiCl4↑+TiCl2回答下列问题。
(1)某同学所画基态 Cl-的外围电子排布图为![]() ,这违反了____________
,这违反了____________
(2)从结构角度解释 TiCl3中Ti(III)还原性较强的原因____________。
(3)钛的氯化物的部分物理性质如下表:
氯化物 | 熔点/℃ | 沸点/℃ | 溶解性 |
TiCl4 | -24 | 136 | 可溶于非极性的甲苯和氯代烃 |
TiCl2 | 1035 | 1500 | 不溶于氯仿、乙醚 |
①TiCl4与TiCl2的晶体类型分别是____________。
②TiCl4与SO42-互为等电子体,因为它们____________相同;SO42-中心原子以3s轨道和3p轨道杂化。
(4)Ti的配合物有多种。Ti(CO)6、Ti(H2O)63+、TiF62-的配体所含原子中电负性最小的是__________;Ti(NO3)4的球棍结构如图,Ti的配位数是_____________
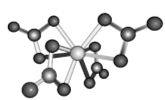
(5)钙钛矿(CaTiO3)是自然界中的一种常见矿物,其晶胞结构如图:
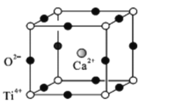
①设N为阿伏加德罗常数的值,计算一个晶胞的质量为______________g.
②假设O2-采用面心立方最密堆积,Ti4+与O2-相切,则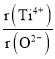 =_________。
=_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列图示所得出的结论正确的是( )
A.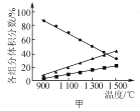 图甲表示H2S(g)受热分解时各组分体积分数随反应温度的变化关系,说明反应生成H2和S
图甲表示H2S(g)受热分解时各组分体积分数随反应温度的变化关系,说明反应生成H2和S
B.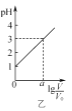 图乙表示V0 mL 0.1 mol·L-1的盐酸加水稀释至V mL,溶液的pH随lg
图乙表示V0 mL 0.1 mol·L-1的盐酸加水稀释至V mL,溶液的pH随lg![]() 的变化关系,则a=2
的变化关系,则a=2
C.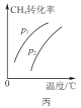 图丙表示密闭容器中CH4(g)+H2O(g)
图丙表示密闭容器中CH4(g)+H2O(g)![]() CO(g)+3H2(g)到达平衡时,CH4的转化率与压强、温度的变化关系曲线,说明p1>p2
CO(g)+3H2(g)到达平衡时,CH4的转化率与压强、温度的变化关系曲线,说明p1>p2
D.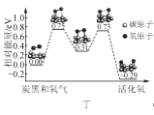 图丁表示炭黑作用下O2生成活化氧过程中能量变化情况,说明每活化一个氧分子吸收0.29 eV的能量
图丁表示炭黑作用下O2生成活化氧过程中能量变化情况,说明每活化一个氧分子吸收0.29 eV的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组数据中,前者刚好是后者两倍的是 ( )
A. 2 mol H2O的摩尔质量和1 mol H2O的摩尔质量
B. 200 mL 1 mol·L-1氯化钙溶液中c(Cl-)和100 mL 2 mol·L-1氯化钾溶液中c(Cl-)
C. 64 g二氧化硫中氧原子数和标准状况下22.4 L一氧化碳中氧原子数
D. 20% NaOH溶液中NaOH的物质的量浓度和10% NaOH溶液中NaOH的物质的量浓度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com