
| A. | 同温同压下,相同体积的物质,它们的物质的量必相等 | |
| B. | 1 L一氧化碳气体一定比1 L氧气的质量小 | |
| C. | 28 g N2和CO的混合气体在标准状况下的体积约为22.4 L | |
| D. | 常温常压下,1 mol碳完全燃烧消耗22.4 L氧气 |
分析 A.必须指出物质的状态为气体,否则该关系不成立;
B.没有指出相同条件下,无法判断二者物质的量大小;
C.标准状况下气体摩尔体积约为22.4L/mol,根据V=nVm计算;
D.常温常压下,不能使用标准状况下的气体摩尔体积计算.
解答 解:A.同温同压下,相同体积的气体,它们的物质的量必相等,物质状态必须为气态,故A错误;
B.缺少条件,无法比较一氧化碳和氧气的物质的量大小,故B错误;
C.N2和CO的摩尔质量都是28g/mol,28 g N2和CO的混合气体的物质的量为1mol,在标准状况下的体积约为22.4 L/mol×1mol=22.4L,故C正确;
D.1 mol碳完全燃烧消耗1mol氧气,1mol氧气在常温常压下的体积大于22.4L,故D错误;
故选C.
点评 本题考查了物质的量的计算,题目难度不大,明确气体摩尔体积的使用条件为解答关键,注意掌握物质的量与其它物理量之间的关系,试题培养了学生的分析能力及化学计算能力.


 优生乐园系列答案
优生乐园系列答案科目:高中化学 来源: 题型:解答题
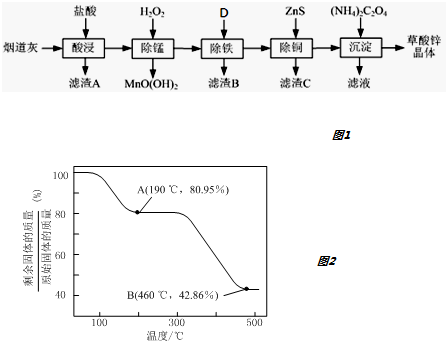
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 | 4.2 | 5.4 |
| 沉淀完全的pH | 3.3 | 9.7 | 6.7 | 8.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤ | B. | ②③⑤④① | C. | ⑤①②③④ | D. | ⑤③②①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在反应中不一定所有元素的化合价都发生变化 | |
| B. | 肯定有一种元素被氧化,另一种元素被还原 | |
| C. | 非金属单质在反应中只做氧化剂 | |
| D. | 某元素从化合物变为单质时,该元素一定被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 滴定次数 | 待测液体积/mL | 标准盐酸体积/mL | |
| 滴定前读数 | 滴定后读数 | ||
| 第1次 | 20.00 | 4.10 | 29.10 |
| 第2次 | 20.00 | 0.00 | 24.90 |
| 第3次 | 20.00 | 4.00 | 29.10 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com