

| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Ca(OH)2 |
| 开始沉淀pH | 1.5 | 3.3 | 12.0 |
分析 CaO、Fe2O3、Al2O3和HCl反应溶解,而SiO2和HCl不反应,不能溶解,此时溶液中除了Ca2+外,还含有Fe3+、Al3+杂质,需除去Fe3+、Al3+但不能损失Ca2+,加NaOH,Fe3++3OH-═Fe(OH)3↓、Al3++3OH-═Al(OH)3↓,除去Fe3+、Al3+,加NaOH需将溶液的pH控制在9~10,否则氢氧化钙沉淀,过滤得沉淀氢氧化铝和氢氧化铁的混合物,然后向混合体系中加入过量的氢氧化钠,氢氧化铝溶解得到偏铝酸盐,向滤液中通入过量的二氧化碳气体得氢氧化铝沉淀,然后灼烧得到氧化铝;
(1)榴石矿可以看做CaO、Fe2O3、Al2O3、SiO2组成,榴石矿加盐酸溶解后,CaO、Fe2O3、Al2O3和HCl反应溶解,而SiO2和HCl不反应,不能溶解;
(2)当NaOH过量时,溶液碱性增强,Al(OH)3会溶解,从氢氧化物沉淀的pH表中可看出,Ca(OH)2在pH为12时开始沉淀,所以碱性增强Ca(OH)2会沉淀;
(3)①浓盐酸易挥发出氯化氢气体溶于水得到稀盐酸,可以和难溶于水的碳酸钙反应生成易溶于水的氯化钙;在实验装置甲和装置乙之间增加除去CO2中含有HCl气体的装置,根据NaHCO3溶液能与HCl气体反应,而不与二氧化碳反应分析;
②根据沉淀溶解平衡的书写方法写出,注意固体稀溶液的标注方法.
解答 解:(1)榴石矿加盐酸溶解,CaO、Fe2O3、Al2O3和HCl反应溶解,反应方程式分别为:MgO+2HCl=MgCl2+H2O,Fe2O3+6HCl=2FeCl3+3H2O,Al2O3+6HCl=2AlCl3+3H2O.而SiO2不与盐酸反应,以沉淀的形式除去,故答案为:Fe3+、Al3+;
(2)由(1)知,此时溶液中除了Ca2+外,还含有Fe3+、Al3+杂质,需除去Fe3+、Al3+但不能损失Ca2+,加NaOH,Fe3++3OH-═Fe(OH)3↓、Al3++3OH-═Al(OH)3↓,除去Fe3+、Al3+,加NaOH需将溶液的pH控制在9~10,若pH过高,会导致生成的Al(OH)3发生反应Al(OH)3+OH-=AlO2-+2H2O溶解,Ca(OH)2在pH为12时开始沉淀,所以碱性增强Ca(OH)2会沉淀,同时Ca2+也因转化为沉淀而损失,
故答案为:Al(OH)3;Ca(OH)2;
(3)①实验室通常用稀盐酸与大理石(或石灰石)反应制取二氧化碳,反应的方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑,因盐酸易挥发出,盐酸是强酸,通入装置乙中的二氧化碳中含有盐酸,溶于水得到稀盐酸可以和难溶于水的碳酸钙反应生成易溶于水的氯化钙,所以没有沉淀产生,在实验装置甲和装置乙之间增加除去CO2中含有HCl气体的装置,NaHCO3溶液能与盐酸反应生成氯化钠、水和二氧化碳,在除去氯化氢的同时增加了二氧化碳的量,
故答案为:盐酸挥发,制取的二氧化碳中含有盐酸;在甲与乙之间加一盛有饱和碳酸氢钠溶液的洗气瓶;
②将二氧化碳气体通入澄清石灰水中,石灰水变浑浊,得到碳酸钙沉淀,碳酸钙的溶解平衡为CaCO3(s)?Ca2+(aq)+CO32-(aq),
故答案为:CaCO3(s)?Ca2+(aq)+CO32-(aq).
点评 本题主要考查了元素化合物中金属铝、铁、非金属碳的性质,解题时不仅需熟知物质间的反应原理,还需灵活运用于实验的设计,题目难度中等.


 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | Al13与Al14互为同素异形体 | |
| B. | Al13超原子中Al原子间是通过离子键结合的 | |
| C. | Al14与氢碘酸反应的化学方程式可表示为:Al14+2HI=Al14I2+H2↑ | |
| D. | Al13在一定条件下能和镁作用生成Mg(Al13)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 草酸(H2C2O4)是一种重要的化工产品.草酸晶体的组成可用H2C2O4•xH2O表示,为了测定x值进行如下实验:
草酸(H2C2O4)是一种重要的化工产品.草酸晶体的组成可用H2C2O4•xH2O表示,为了测定x值进行如下实验:查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 湿法 | 强碱介质中,Fe(NO3)3与NaClO反应得到紫红色高铁酸盐溶液 |
| 干法 | Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸钾(K2FeO4)和KNO2等产物 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 红热的铁丝在氧气中燃烧,火星四射,生成黑色固体颗粒 | |
| B. | 钠在空气中燃烧,发出黄色的火焰,生成淡黄色固体 | |
| C. | 氢气在氯气中安静燃烧,生成白烟 | |
| D. | 点燃的硫在氧气中剧烈燃烧,发出蓝紫色火焰 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
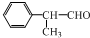 ,工业合成路线如下:
,工业合成路线如下: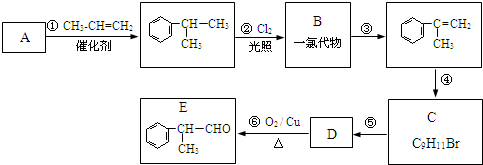
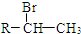
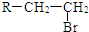 .(R-代表烃基)
.(R-代表烃基)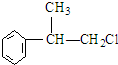 、
、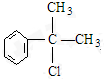 ;
;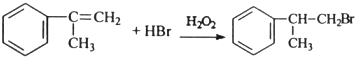 ;
;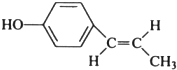 (只写反式结构).
(只写反式结构).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com