
【题目】有铁的氧化物样品,用150 mL 5 mol/L的盐酸恰好使其完全溶解,所得溶液还能吸收标准状况下氯气1.68L,使其中的Fe2+全部转化为Fe3+,该样品可能的化学式是( )
A.Fe2O3B.Fe3O4C.Fe5O7D.Fe4O5
【答案】D
【解析】
n(HCl)=0.15 L× 5mol/L=0.75 mol,n(Cl2)=![]() =0.075mol,反应中HCl的H元素与氧化物中O元素全部结合生成H2O,反应后溶液成分为FeCl3,结合质量守恒计算。
=0.075mol,反应中HCl的H元素与氧化物中O元素全部结合生成H2O,反应后溶液成分为FeCl3,结合质量守恒计算。
反应中HCl的H元素与氧化物中O元素全部结合生成H2O,则氧化物中n(O)=![]() ×n(HCl)=
×n(HCl)= ![]() ×0.75mol=0.375mol,反应后溶液成分为FeCl3,n(Cl-)=0.75mol+0.075mol×2=0.9 mol,则n(Fe)=0.9mol×
×0.75mol=0.375mol,反应后溶液成分为FeCl3,n(Cl-)=0.75mol+0.075mol×2=0.9 mol,则n(Fe)=0.9mol×![]() =0.3mol,所以:n(Fe):n(O)=0.3mol:0.375mol=4:5,该氧化物的化学式为Fe4O5,D项正确,
=0.3mol,所以:n(Fe):n(O)=0.3mol:0.375mol=4:5,该氧化物的化学式为Fe4O5,D项正确,
答案选D。


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案科目:高中化学 来源: 题型:
【题目】Ⅰ、在528K、固定计提的容器中,反应CO(g)+2H2(g)CH3OH(g)过程中能量变化如图所示,曲线Ⅱ表示使用催化剂时的能量变化,若投入a molCO、2amolH2,平衡时能生成0.1amolCH3OH,反应就具工业应用价值。
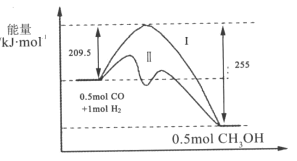
(1)该反应的热化学方程式为______;
(2)若按上述投料比使该反应具有工业应用价值,CO的平衡转化率为______;
(3)在容器容积不变的前提下,欲提高H2的转化率,可采取的措施______;(答出两项即可)
(4)关于反应历程Ⅰ与反应历程Ⅱ相比较,下列说法正确的是______;
A.反应历程Ⅱ比反应历程Ⅰ放出的热量少
B.反应历程Ⅱ比反应历程Ⅰ反应速率快
C.反应历程Ⅱ比反应历程Ⅰ平衡常数小
D.反应历程Ⅱ和反应历程Ⅰ中CO转化率相同
Ⅱ、已知:N2(g)+3H2(g)2NH3(g)△H=-92.1kJ/mol,在容器中充入1.4mol/LN2与4 mol/LH2,其中N2与NH3在达到平衡后改变某条件下的浓度变化如图所示
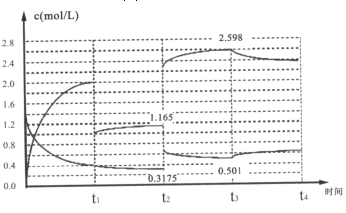
(5)t2时刻改变的条件为______;
(6)t2=t3时刻的平衡常数为______(mol/L)-2。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】核内中子数为N的R2+,质量数为A,则ng它的同价态氧化物中所含电子物质的量为( )
A.![]() (A+N-10)molB.
(A+N-10)molB.![]() (A-N+6)mol
(A-N+6)mol
C.(A-N+2)molD.![]() (A-N+8)mol
(A-N+8)mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过量铝粉分别与下列4种等体积的溶液充分反应,放出氢气最多的是( )
A.3mol·L-1H2SO4溶液B.18mol·L-1H2SO4溶液
C.1.5 mol·L-1KOH溶液D.3mol·L-1HNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由Al、CuO、Fe2O3组成的混合物共10.0g,放入500mL某浓度的盐酸中,混合物完全溶解,当再加入250mL 2.00mol/L的NaOH溶液时,得到沉淀最多。上述盐酸的浓度为( )
A. 1.00 mol/LB. 0.500 mol/L
C. 2.00 mol/LD. 3.00 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是很好的净水剂,高铁酸钡( BaFeO4)是高能电池阳极的优良材料。已知:K2FeO4为紫色固体,微溶于KOH溶液,在酸性或中性溶液中能快速产生O2,在碱性溶液中较稳定;在碱性溶液中,NaCl、NaNO3、K2FeO4的溶解性都小于Na2FeO4;BaFeO4难溶于水和碱性溶液。某化学兴趣小组欲制取“84”消毒液,进而制取少量K2FeO4和 BaFeO4。请回答下列问题:
(实验一)选择合适的仪器和试剂制取氯气,进而制备高浓度的“84”消毒液。

(1)选择合适的仪器,导管接口正确的连接顺序为___________;所选装置(A或B)中发生反应的离子方程式为______________________。
(实验二)用“84”消毒液制取K2FcO4
实验步骤:①用如图所示装置(夹持仪器略去)使反应物充分反应;②用砂芯漏斗对烧杯中的溶液进行抽滤,向滤液中慢慢加入KOH溶液;③再用砂芯漏斗对步骤②的最后反应混合物进行抽滤,并用苯、乙醚洗涤沉淀,真空干燥后得K2FeO4。

(2)写出步骤①中物质在20℃冷水浴中发生反应的化学方程式:______________________。
(3)步骤②中能够发生反应的原因是______________________,步骤③中不用水,而用苯、乙醚洗涤沉淀的目的是_________________________________。
(实验三)将上述产品配成K2FeO4碱性溶液,再慢慢加入Ba(OH)2溶液,抽滤得 BaFeO4。
(4)若投入ag硝酸铁晶体,得到bg高铁酸钡,则高铁酸钡的产率是___________。[已知Fe(NO3)3·9H2O的摩尔质量为404g·mol-1, BaFeO4的摩尔质量为257g·mol-1]
(实验四)利用如图所示电解装置也可以制得 BaFeO4。

(5)在___________(填“阳极区”或“阴极区”)可得到高铁酸钡,阳极的电极反应式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将5g碳酸钠、碳酸氢钠和氢氧化钠的固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入2mol·L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如图所示:

(1)写出OA段所发生反应的离子方程式____、____。
(2)当加入45mL盐酸时,产生CO2的体积为___mL(标准状况)。
(3)混合物中氢氧化钠质量分数是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷、乙烯是重要的化工原料。下列叙述正确的是
A. 甲烷、乙烯是同分异构体
B. 可用酸性高锰酸钾溶液来区别甲烷和乙烯
C. 甲烷与氯气在光照条件下发生置换反应
D. 乙烯与水在一定条件下发生取代反应生成乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】G是一种新型可降解的生物高分子材料,以丙烯(CH2=CH﹣CH3)为主要原料合成G的流程路线如图所示:
![]()
(1)聚合物G的结构简式是_____。
(2)E分子中含氧官能团的名称是_____。
(3)A转化为B的化学方程式是_____。
(4)C有多种同分异构体,写出其中能发生水解反应的有机物的结构简式_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com