
 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
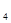 >H
>H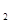 Y0
Y0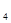 >H
>H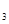 X0
X0 ,下列判断正确的是( )
,下列判断正确的是( )| A.①②④ | B.②③ | C.①②③ | D.①②③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.X、Y、Z的原子半径大小:X>Y>Z |
| B.Y、Z的气态氢化物中,前者更稳定 |
| C.Z、W的最高价氧化物对应水化物的酸性,前者更强 |
| D.X、W的气态氢化物相互反应,生成物中既含离子键又含共价键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
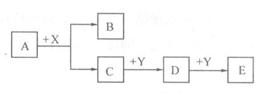
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.MgCl2 | B.NaBr | C.HCl | D.NaI |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
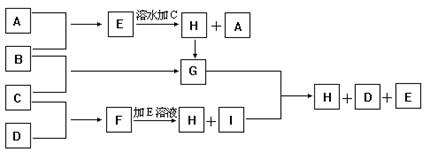
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 后,得到气体的质量之比是____________________________。
后,得到气体的质量之比是____________________________。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com