
| A. | 氯化铝溶液中加入过量氨水:Al3++3NH3.H2O=Al(OH)3↓+3NH4+ | |
| B. | 碳酸钙和盐酸反应:CO32-+2H+=CO2↑+H2O | |
| C. | 三氯化铁溶液与氢氧化钠溶液反应:FeCl3+3OH-=Fe(OH)3↓+3Cl- | |
| D. | 铜加入稀硝酸中:Cu+4H++NO3-=Cu2++NO↑+2H2O |
分析 A.反应生成氢氧化铝和氯化铵;
B.碳酸钙在离子反应中保留化学式;
C.氯化铁完全电离,氯离子实际不参加反应;
D.电子、电荷不守恒.
解答 解:A.氯化铝溶液中加入过量氨水的离子反应为Al3++3NH3.H2O=Al(OH)3↓+3NH4+,故A正确;
B.碳酸钙和盐酸反应的离子反应为CaCO3+2H+=Ca2++CO2↑+H2O,故B错误;
C.三氯化铁溶液与氢氧化钠溶液反应的离子反应为Fe3++3OH-=Fe(OH)3↓,故C错误;
D.铜加入稀硝酸中的离子反应为3Cu+8H++2NO3-3=Cu2++2NO↑+4H2O,故D错误;
故选A.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应、复分解反应的离子反应考查,注意电子、电荷守恒的分析及离子反应中保留化学式的物质,题目难度不大.


 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | H+、I-、NO3-、CO32- | B. | NH4+、Fe3+、OH-、Br- | ||
| C. | K+、Cl-、Cu2+、NO3- | D. | Al3+、SO42-、Na+、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生成水蒸气体积为6.72m/NA L | B. | 参加反应的氨气为m/5 mol | ||
| C. | 生成NO的质量为6mNA g | D. | 发生还原反应的原子数为m/2 个 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
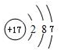 ;元素③的最低价氢化物的电子式为
;元素③的最低价氢化物的电子式为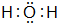 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2═CH2+HCl→CH3CH2Cl | B. | 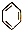 +HO-NO2$→_{55~60℃}^{浓H_{2}SO_{4}}$ +HO-NO2$→_{55~60℃}^{浓H_{2}SO_{4}}$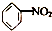 +H2O +H2O | ||
| C. | nCH2═CH2$\stackrel{一定条件}{→}$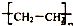 | D. | (C6H10O5)n+nH2O$\stackrel{一定条件}{→}$nC6H12O6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com