
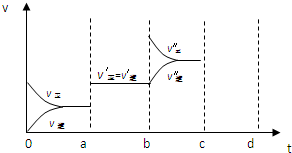 ��25��ʱ��2L���ܱ�������A��B��C��������ij�ʼŨ�Ⱥ�ƽ��Ũ�����±���
��25��ʱ��2L���ܱ�������A��B��C��������ij�ʼŨ�Ⱥ�ƽ��Ũ�����±���| ���� | A | B | C |
| ��ʼŨ��/mol?L-1 | 1.0 | 2.0 | 0 |
| 2minʱ��ƽ��Ũ��/mol?L-1 | 0.4 | 0.2 | 1.2 |
| ������ |
| ��ʼ�� |
| ��c |
| ��t |
| ������ƽ��Ũ���ݴη��˻� |
| ��Ӧ��ƽ��Ũ���ݴη��˻� |
| 0.6mol/L |
| 1.0mol/L |
| 0.6mol/L |
| 2min |
| 1.2 2 |
| 0.4��0.2 3 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
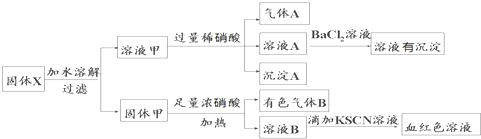
| A������A��һ����NO����CO2 |
| B����������ҺA�м���BaCl2��Һ�г����������ó���ΪBaSO3 |
| C�����������м�������Ũ���ᣬ�ټ�KSCN��Һ��û��Ѫ��ɫ����֤��ԭ�������һ��û��Fe2O3 |
| D������X��һ������K2SiO3��K2SO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����״���£�1.12 L NO��1.12 L O2��Ϻ����������к��е�ԭ����Ϊ0.2NA |
| B��ͬһ�¶��£�1 L 0.5 mol?L-1��NH4Cl��Һ��2 L 0.25 mol?L-1��NH4Cl��Һ����NH4+���������С��0.5NA |
| C��27 g Al�ڱ�״���µ�22.4 L Cl2��ȼ�գ�ת�Ƶĵ�������Ϊ3N |
| D��1 L 0.5 mol?L-1 FeCl3��Һ��ȫˮ���Fe��OH��3����������ĿΪ0.5NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��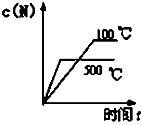 |
B��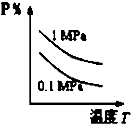 |
C��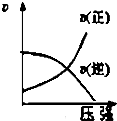 |
D��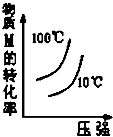 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ڢۢ� | B���ڢۢ� |
| C���٢ܢ� | D���٢ڢۢܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 |
| 4 |
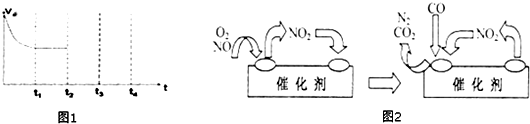
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1��2��3 |
| B��6��3��2 |
| C��3��1��1 |
| D��1��1��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
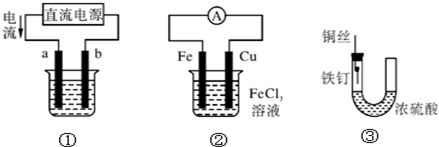
| A����װ�âپ���ͭ����a��Ϊ��ͭ���������ҺΪCuSO4��Һ |
| B����װ�âٽ��е�ƣ��Ƽ�����b���� |
| C��װ�âڵ��ܷ�Ӧ�ǣ�Cu+2Fe3+�TCu2++2Fe2+ |
| D��װ�â��е���������û����ʴ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ϩ�Ľṹ��ʽ��CH2CH2 |
| B����ϩ�ķ���ʽ��C2H4 |
| C������Ľṹ��ʽ��C2H4O2 |
D����ȩ�ĵ���ʽ��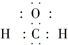 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com