
下列有关滴定操作的顺序正确的是( )
①用标准溶液润洗滴定管 ②往滴定管内注入标准溶液 ③检查滴定管是否漏水 ④滴定 ⑤洗涤
A.⑤①②③④B.③⑤①②④ C.⑤②③①④ D.②①③⑤④
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)4.2一次电池二次电池试卷(解析版) 题型:选择题
被称之为“软电池”的纸质电池,采用一个薄层纸片(在其一边镀锌,而在其另一边镀二氧化锰)作为传导体。在纸内的离子“流过”水和氧化锌组成的电解液。电池总反应为:Zn+2MnO2+H2O ZnO+2MnO(OH),下列说法正确的是( )
ZnO+2MnO(OH),下列说法正确的是( )
A.该电池的正极为锌
B.该电池反应中二氧化锰起催化剂作用
C.当0.1 mol Zn完全溶解时,转移电子个数为1.204×1024
D.电池正极反应式为:2MnO2+2e-+2H2O 2MnO(OH)+2OH-
2MnO(OH)+2OH-
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)3.3盐类水解的原理试卷(解析版) 题型:选择题
在一定条件下,Na2CO3溶液存在水解平衡:C+H2O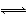 HC+OH-。下列说法正确的是( )
HC+OH-。下列说法正确的是( )
A.稀释溶液,水解平衡常数增大
B.通入CO2,平衡向正反应方向移动
C.升高温度,减小
D.加入NaOH固体,溶液pH减小
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)3.2水的电离溶液的酸碱性(解析版) 题型:选择题
室温下,某溶液中由水电离产生的c(H+)等于10-13 mol·L-1,该溶液的溶质不可能是( )
A.NaHSO4B.NaCl C.HClD.Ba(OH)2
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)3.2.3 酸碱中和滴定(解析版) 题型:选择题
中和滴定实验中,标准NaOH溶液的浓度通常用H2C2O4·H2O为基准物质进行标定。基准物质必须具备的条件:①物质纯度要高,②相对分子质量较大,③性质稳定,如不易分解、不风化、不潮解、不跟空气中的CO2、O2等反应。实验室标定盐酸的浓度时,选择的基准物质最好是( )
A.NaOH B.NaHCO3 C.Na2CO3 D.Na2CO3·10H2O
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)3.2.2 pH的计算试卷(解析版) 题型:选择题
水的电离平衡曲线如下图所示,下列说法不正确的是( )
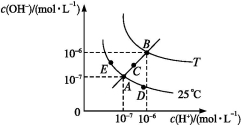
A.图中五点KW间的关系:B>C>A=D=E
B.若从A点到D点,可采用:温度不变在水中加入少量的酸
C.若从A点到C点,可采用:温度不变在水中加入适量的NH4Cl固体
D.若处在B点时,将pH=2的硫酸与pH=10的KOH等体积混合后,溶液显中性
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)3.1弱电解质的电离试卷(解析版) 题型:填空题
在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力如下图所示,请回答:

(1)“O”点导电能力为0的理由是 。
(2)A、B、C三点溶液c(H+)由小到大的顺序为 。
(3)若使C点溶液中c(CH3COO-)增大的同时溶液的c(H+)减小,可采取的措施是:
① ;② ;③ 。
(4)经实验测得C点处:c(CH3COOH)=0.1 mol·L-1,c(CH3COO-)=0.01 mol·L-1,则该条件下CH3COOH的电离常数Ka= 。
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)2.3.3化学平衡常数试卷(解析版) 题型:选择题
关于平衡常数,下列说法不正确的是( )
A.平衡常数不随反应物或生成物的浓度的改变而改变
B.平衡常数随温度的改变而改变
C.平衡常数随压强的改变而改变
D.使用催化剂不能使平衡常数增大
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学铜及其化合物主要性质、合金(解析版) 题型:选择题
下列推断正确的是
| 事实 | 结论 |
A | 常温下铁、铜均不溶于浓硫酸 | 常温下铁、铜与浓硫酸均不反应 |
B | HCl与Na2CO3溶液反应生成CO2 | 可用饱和Na2CO3溶液除去CO2中的少量HCl |
C | 氧化铜高温下生成红色物质,该物质可与稀硫酸反应 | 氧化铜高温下可分解生成Cu2O |
D | 稀、浓硝酸分别与铜反应,还原产物分别为NO和NO2 | 稀硝酸氧化性比浓硝酸强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com