
【题目】在300mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:
Ni(s)+4CO(g)![]() Ni(CO)4(g),已知该反应平衡常数与温度的关系如下表:
Ni(CO)4(g),已知该反应平衡常数与温度的关系如下表:
温度/℃ | 25 | 80 | 230 |
平衡常数 | 5×104 | 2 | 1.9×10-5 |
下列说法不正确的是
A. 上述生成Ni(CO)4(g)的反应为放热反应
B. 在80℃时,测得某时刻,Ni(CO)4、CO浓度均为0.5mol/L,则此时V(正)>V(逆)
C. 25℃时反应Ni(CO)4(g)![]() Ni(s)+4CO(g)的平衡常数为2×10-5 (mol·L-1)3
Ni(s)+4CO(g)的平衡常数为2×10-5 (mol·L-1)3
D. 80℃达到平衡时,测得n(CO)=0.3mol,则Ni(CO)4的平衡浓度2 mol/L。
【答案】B
【解析】A.由表中数据可知,温度越高平衡常数越小,说明升高温度平衡向逆反应移动,升高温度平衡向吸热反应移动,故正反应为放热反应,A正确;B.浓度商Qc=0.5/0.54=8,大于80℃平衡常数2,故反应进行方向逆反应进行,故v(正)<v(逆),B错误;C. 25℃时反应Ni(s)+4CO(g)Ni(CO)4(g)的平衡常数为5×104,相同温度下,对于同一可逆反应的正、逆反应平衡常数互为倒数,故25°C时反应Ni(CO)4(g)Ni(s)+4CO(g)的平衡常数为1/5×104=2×10-5,C正确;D. 80℃达到平衡时,测得n(CO)=0.3mol,c(CO)=0.3mol/0.3L=1mol/L,故c[Ni(CO)4]=Kc4(CO)=2×14mol/L=2mol/L,D正确;答案选B。


科目:高中化学 来源: 题型:
【题目】常温时,发生反应:AsO33-(aq)+I2(aq)+2OH-(aq)![]() AsO43-(aq)+2I-(aq)+H2O(l) △H。溶液中c(AsO43-) 与反应时间(t)的关系如图所示。下列说法正确的是( )
AsO43-(aq)+2I-(aq)+H2O(l) △H。溶液中c(AsO43-) 与反应时间(t)的关系如图所示。下列说法正确的是( )

A. t1时v逆小于t2时v逆
B. 该反应达到平衡时,2v生成(I-)=v生成(AsO33-)
C. 升高温度,c(AsO33-) 浓度增大,则△H>0
D. 增大c(OH-),平衡向正反应方向移动,平衡常数变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、下图是全钒液流电池的示意图

该电池充放电的总反应式为:
![]()
请回答下列问题:
(1)充电时的阴极反应式为______________,阳极附近颜色变化是______。
(2)放电过程中,正极附近溶液的pH ________(选填“升高”“降低”或“不变”)。
II、回收利用废钒催化剂(主要成分为V2O5、VOSO4和二氧化硅)的工艺流程如下图所示。

(3)滤渣可用于______________________(填一种用途)。
(4)25℃时,取样进行实验分析,得到钒沉淀率和溶液pH之间的关系如下表所示:
pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
钒沉淀率(%) | 88.1 | 91.8 | 96.5 | 98 | 99.8 | 97.8 | 96.4 | 93.0 | 89.3 |
根据上表数据判断,加入氨水调节酸碱性,溶液的最佳pH为____;上述过滤操作过程中所需用到的玻璃仪器有__________________________________。
(5)为了提高钒的浸出率,用酸浸使废钒催化剂中的V2O5转变成可溶于水的VOSO4,酸浸过程中,氧化产物和还原产物的物质的量之比为________。
(6)氧化过程中,VO2+变为VO2+,则该反应的离子方程式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是
A. 0.1mol/L醋酸溶液中含有醋酸分子的数目为0.1NA
B. 25℃时,1LpH=12的Na2CO3溶液中含有Na+的数目为0.2NA
C. 常温下,20LpH=12的Na2CO3溶液中含有OH-数目为0.2NA
D. 某密闭容器盛有0.1molN2和0.3molH2,在一定条件下充分反应,转移电子数目为0.6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲~庚等元素在周期表中的相对位置如下表,己的最高价氧化物的水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数。下列判断正确的是( )
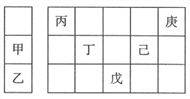
A. 丙与戊的原子序数相差25 B. 气态氢化物的稳定性:庚<己<戊
C. 丁的最高价氧化物可用于制造光导纤维 D. 常温下,甲和乙的单质能与水剧烈反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《本草纲目》记载了烧酒的制造工艺:“凡酸坏之酒,皆可蒸烧”,“ 以烧酒复烧二次……价值数倍也”。请你分析、对比此方法与分离下列物质的实验方法在原理上相同的是
A. 苯和溴苯 B. 硝酸钾和氯化钠 C. 食盐水和泥沙 D. 甲苯和水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由煤制合成气(组成为H2、CO和CO2)制备甲醇或二甲醚是我国保障能源安全战略的重要措施。
(1)以澄清石灰水、无水硫酸铜、浓硫酸、灼热氧化铜为试剂检验合成气中含有H2、CO和CO2三种气体,所选用试剂及使用顺序为_______________________。
(2)制备甲醇(CH3OH)、二甲醚(CH3OCH3)主要过程包括以下四个反应:

①由H2 和CO可直接制备二甲醚:2CO(g)+ 4H2(g)==CH3OCH3(g)+H2O(g) ΔH=_____________。
分析上述反应(均可逆),二甲醚合成反应对于CO转化率的影响是_____________(填“增大”“ 减小”或“无影响”),其理由是______________________。
②有研究者用Cu -Zn –Al和Al2O3作催化剂。在压强为5.0Mpa的条件下,由合成气[![]() =2]直接副备二甲醚,结果如图所示。
=2]直接副备二甲醚,结果如图所示。

290℃时二甲醚的选择性(选择性=![]() ×100% 10)为97.8%,则290 ℃时二甲醚的产率为_______________________。
×100% 10)为97.8%,则290 ℃时二甲醚的产率为_______________________。
(3)在一个固定容积的密闭容器中,发生水煤气变换反应。
①下列各项能判断该反应已达到化学平衡状态的是________________(填字母)。
a.容器中压强不变 b. ΔH不变 c.V正(H2 )=v逆(CO) d.CO的质量分数不变
②温度为850℃时,该反应的平衡常数K=1,反应过程中各物质的浓度变化如下表:
时间/min | CO | H2O | CO2 | H2 |
0 | 0.200 | 0.300 | 0 | 0 |
2 | 0.138 | 0.238 | 0.062 | 0.062 |
3 | c1 | c2 | c3 | c4 |
4 | c1 | c2 | c3 | c4 |
5 | 0.065 | 0.21 | 0.125 |
0~4 min时,H2O(g)的转化率=______。表中4~5 min之间数值发生变化,可能的原因是___________
(填字母)。
a增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com