

分析 (1)根据量取液体体积的精确度以及液体的性质选择仪器;在烧杯中稀释溶液;用容量瓶配制一定浓度的溶液;
(2)①滴定管清洗完之后管壁上残留水,会使待测溶液浓度下降;
②由图象上可知随氨水体积的增大,导电性先增大后减小,结合醋酸与氨水反应过程分析解答;
③根据图表可知当混合液导电能力最强时,醋酸恰好与氨水反应完全,分别求出反应消耗的醋酸的物质的量和氨水的物质的量,依据酸碱中和反应n(CH3COOH)=n(NH3•H2O)计算求解.
解答 解:(1)滴定管精确度为0.01ml,醋酸具有酸性能腐蚀橡胶管,所以应选用酸式滴定管量取白醋;然后把白醋,转移到烧杯中加水稀释溶液,再把溶液转入100mL容量瓶中中定容;
故答案为:酸式滴定管;烧杯;容量瓶;
(2)①为防止滴定管清洗完之后管壁上残留水将待测液稀释,应用所盛0.1000mol•L-1的氨水润洗2-3次,
故答案为:0.1000mol•L-1的氨水;防止氨水被稀释;
②醋酸为弱电解质,开始导电性不强,滴入稀氨水,反应生成醋酸铵,为强电解质,离子浓度增大,导电性增强,继续滴入氨水,体积变大,离子浓度减小,导电性又逐渐减弱;
故答案为:醋酸为弱电解质,开始导电性不强,滴入稀氨水,反应生成醋酸铵,为强电解质,离子浓度增大,导电性增强,继续滴入氨水,体积变大,离子浓度减小,导电性又逐渐减弱;
③设白醋的浓度为C,则反应消耗的醋酸的物质的量为n(CH3COOH)=C×10.00mL×$\frac{20}{100}$;反应消耗的氨水的物质的量为:n(NH3•H2O)=0.1000mol•L-1×20ml,根据图表可知当混合液导电能力最强时,醋酸恰好与氨水反应完全,所以n(CH3COOH)=n(NH3•H2O),即C×10.00mL×$\frac{20}{100}$=0.1000mol•L-1×20ml,C=1.000mol•L-1;
故答案为:1.000mol•L-1.
点评 本题考查溶液的配制、中和滴定实验,题目难度中等,注意滴定管的选择和使用的注意事项,溶液的导电性取决于溶液中离子的浓度,侧重于考查学生的实验操作能力.


 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源:2017届湖北省荆门市高三上九月联考化学试卷(解析版) 题型:推断题
有机化合物G常用作香料。合成G的一种路线如下:
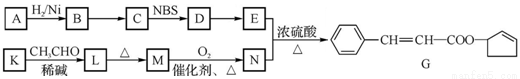
已知以下信息:
① A的分子式为C5H8O,核磁共振氢谱显示其有两种不同化学环境的氢
② CH3CH2CH=CH2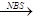 CH3CHBrCH=CH2
CH3CHBrCH=CH2
③ CH3CHO+CH3CHO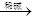
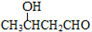 、
、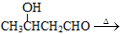 CH3CH=CHCHO+H2O
CH3CH=CHCHO+H2O
回答下列问题:
(1)A的结构简式为______________,D中官能团的名称为____________________。
(2)B→C的反应类型为_______________。
(3)D→E反应的化学方程式为_________________________________。
(4)检验M是否已完全转化为N的实验操作是___________________________。
(5)满足下列条件的L的两种同分异构体有 种(不考虑立体异构)。① 能发生银镜反应 ② 能发生水解反应。其中核磁共振氢谱中有5组峰,且峰面积之比为1:2:2:2:3的结构简式为 。
(6)参照上述合成路线,设计一条以1-丁醇和NBS为原料制备顺丁橡胶(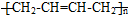 )的合成路线:___________________________。
)的合成路线:___________________________。
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三上第二次月考化学试卷(解析版) 题型:选择题
将等物质的量的镁和铝相混合,取四份等质量的该混合物分别加在足量的下列溶液中,充分反应后,放出氢气最多的是( )
A.3 mol/L HCl B.4 mol/L HNO3 C.8 mol/L NaOH D.18 mol/L H2SO4
查看答案和解析>>
科目:高中化学 来源:2016-2017学年重庆市高一上10月月考化学试卷(解析版) 题型:实验题
过碳酸钠(2Na2CO3·3H2O2)广泛用于洗涤、纺织、医疗、造纸等。某兴趣小组展开了深入的学习:
【资料卡片】:

I、制备研究:工业上采用“醇析法”将其转化成固态的过碳酸钠晶体(化学式为2Na2CO3·3H2O2), “醇析法”的生产工艺流程如下:
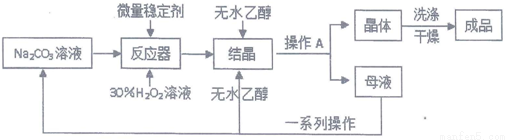
请回答问题:
(1)Na2CO3俗名:_______________;其水溶液能使酚酞变_______________;
(2)H2O2受热容易分解,写出该分解反应的方程式:_________________;
(3)生产过程中,反应及干燥均需在低温度下进行,原因是________________;
(4)生产过程中,加入较多无水乙醇后,过碳酸钠晶体大量析出,此无水乙醇的作用可能是_________________;
(5)操作A的名称是______________,若在实验室完成此操作,需要的玻璃仪器是烧杯、玻璃棒和_____________;
(6)母液可以循环使用,但须进行“一系列操作”分离,这些操作包括:加入少量___________,不再有气泡产生后,过滤,将所得滤液再进行______________(填操作名称),即可得Na2CO3溶液和95%的乙醇。为获取无水乙醇,还需进行的操作是:向95%的乙醇中加入足量CaO后,选__________(填序号)装置进行实验。
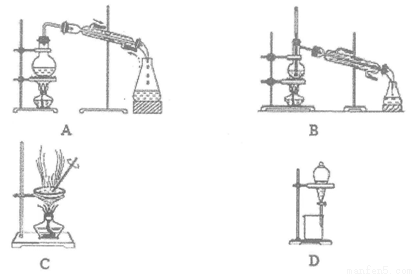
II、纯度测定:兴趣小组同学设计了如图1所示实验装置(部分仪器略去),测定过碳酸钠样品中2Na2CO3·3H2O2的质量分数。步骤如下:
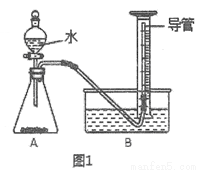
① 连接仪器并检查好气密性
② 将过碳酸钠样品(2.20g)和少许MnO2均匀混合后置于装置A中,在量筒中加满水;
③ 连接仪器,打开滴液漏斗活塞,缓缓滴入水;
④ 待装置A中_____________时,停止滴加水,并关闭活塞;
⑤ 冷却至室温后,平视读数;
⑥ 根据数据进行计算。
请回答下列问题:
(7)完善实验步骤的相关内容:④ __________;
(8)第⑤中,已“冷却至室温”的判断依据是:_____________;
(9)量筒中,加装的长导管的作用是:______________;
(10)实验中,______________,则开始收集气体;
A.刚开始出现气泡时
B.当气泡均匀连续出现时
C.若用带火星木条放在导管口部,复燃时
(11)量筒的局部示意见图2,平视读数时应沿____________视线(选填“a”或“b”) 进行。图中________视线(选填“a”或“b”)对应的读数较大。
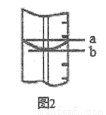
(12)若量筒中收集到气体的体积是224mL (己转化为标准状况下的数据),计算过碳酸钠样品中2Na2CO3·3H2O2的质量分数:_____________;[Mr(O2)=32、Mr(2Na2CO3·3H2O2)=314]
(13)经过讨论,小组同学一致认为测定结果偏大,理由是_________________(任写一种)。
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂.请填写下列空白:
某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂.请填写下列空白:| 滴定次数 | 待测NaOH溶液的体积/mL | 0.100 0 mol•L-1盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 二甲醚(CH3OCH3)是一种重要的清洁燃料,也可替代氟利昂作做冷剂等,对臭氧层无破坏作用.工业上以水煤气(CO、H2)为原料生产二甲醚CH3OCH3的新工艺主要发生三个反应:
二甲醚(CH3OCH3)是一种重要的清洁燃料,也可替代氟利昂作做冷剂等,对臭氧层无破坏作用.工业上以水煤气(CO、H2)为原料生产二甲醚CH3OCH3的新工艺主要发生三个反应:| 化学键 | H-H | C-H | C-O | O-H |
| 键能(kJ.mol-1 | 436 | 414 | 326 | 464 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某氮肥硫酸铵中混有硫酸氢铵.为测定该氮肥的含氮量,一化学研究性学习小组取一定量氮肥样品,研磨使其混合均匀,备用.已知:
某氮肥硫酸铵中混有硫酸氢铵.为测定该氮肥的含氮量,一化学研究性学习小组取一定量氮肥样品,研磨使其混合均匀,备用.已知:| 氢氧化钠溶液体积/mL | 40.00mL | ||
| 样品质量/g | 7.750 | 15.50 | 23.25 |
| 氨气质量/g | 1.870 | 1.870 | 1.700 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com