
| A. | 金属钠投入到硫酸铜的溶液中不能置换得到铜单质 | |
| B. | 金属钠着火燃烧时,可以用水灭火 | |
| C. | 铝比铁活泼,所以铝比铁更容易被腐蚀 | |
| D. | 正常雨水PH等于7,酸雨的PH小于7 |
分析 A、钠和盐溶液反应时,先和水反应,如果能发生复分解反应,则再发生复分解反应;
B、钠与水反应生成氢氧化钠与氢气;
C、根据铝的性质进行分析,铝在空气中易被氧气氧化生成致密的氧化物保护膜;
D、正常的雨水因为溶解了少量的二氧化碳气体而显弱酸性,雨水的pH只是稍小于7,当雨水中溶解了二氧化硫、二氧化氮等物质时,雨水的酸性会明显增强,当达到一定程度时就形成酸雨,pH只是稍小于5.6.
解答 解:A、钠投入硫酸铜溶液时,钠和水反应生成氢氧化钠和氢气,氢氧化钠再和硫酸铜发生复分解反应生成氢氧化铜蓝色沉淀,所以得不到金属单质铜,故A正确;
B、钠与水反应生成氢氧化钠和氢气,则钠失火时不能用水灭火,故B错误;
C、通常情况下铝制品比铁更耐腐蚀,这是因为铝在常温下与空气中的氧气发生化学反应,使铝的表面生成了一层致密的氧化铝薄膜从而阻止了内部的铝进一步氧化,所以铝比铁更容易被腐蚀,故C错误;
D、正常雨水中因为溶有二氧化碳而显酸性,正常雨水的pH约为5.6,但酸雨的pH却小于5.6,故D错误;
故选A.
点评 本题主要考查了有关元素化合物的知识,注意物质的性质决定其用途,难度不大.注意C表面形成致密的氧化膜.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | pH=1 | |
| B. | c(H+)=c(CH3COO-) | |
| C. | 加入少量CH3COONa固体后,醋酸的电离程度减小 | |
| D. | 与0.1 mol•L-1NaOH溶液等体积混合后所得溶液显中性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
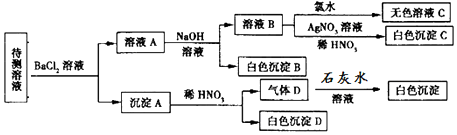
| A. | SO42-、SO32-至少含有一种 | |
| B. | 沉淀B的化学式为BaCO3 | |
| C. | 肯定存在的阴离子有CO32-、HCO3-、Cl- | |
| D. | 肯定没有的离子是Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有的中子数为a+b | B. | 含有的电子数为a-n | ||
| C. | 质量数为a+b+n | D. | 1mol该原子的质量约为bg |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
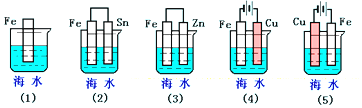
| A. | (5)(2)(1)(3)(4) | B. | (2)(5)(3)(4)(1) | C. | (5)(3)(4)(1)(2) | D. | (1)(5)(3)(4)(2) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应中Ag和H2S均是还原剂,发生氧化反应 | |
| B. | 银针验毒时,空气中的氧气失去电子 | |
| C. | X的化学式为Ag2S,颜色为黑色,通过观察银针颜色变化来判断死者是否中毒 | |
| D. | 每生成1mo1X,反应转移4mo1 e- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com