
| ||
| A、C3N3(OH)3生成HNCO的反应为氧化还原反应 |
| B、生成1 mol N2转移的电子为6 mol |
| C、NO2在反应中被氧化为N2 |
| D、氧化产物与还原产物的物质的量之比为4:3 |
| ||
| 24 |
| 7 |


 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向1mL 1% NaOH溶液加入2mL 2%的CuSO4溶液,振荡后滴加0.5mL葡萄糖溶液,加热 | 未出现红色沉淀 | 葡萄糖中不含有醛基 |
| B | 在CuSO4溶液中加入KI溶液,再加入苯,振荡 | 有白色沉淀生成,苯层呈紫色 | 白色沉淀可能为CuI |
| C | 等体积pH=3的HA和HB两种酸分别与足量的锌反应,排水法收集气体 | HA放出的氢气多且反应速率快 | HA酸性比HB强 |
| D | 向加入了几滴酚酞试液的Na2CO3溶液中滴加BaCl2溶液 | 红色逐渐褪去 | Na2CO3溶液中存在水解平衡 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
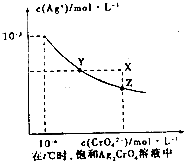 ①已知t℃时AgCl的Kap为2×10-10;②在t℃时,Ag2CrO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
①已知t℃时AgCl的Kap为2×10-10;②在t℃时,Ag2CrO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )| A、在t℃时,反应Ag2CrO4(s)+2Cl-(aq)?2AgCl(s)+CrO42-(aq)的平衡常数K=2.5×107 |
| B、在t℃时,Ag2CrO4的Kap为1×10-9 |
| C、在饱和Ag2CrO4溶液中加入K2CrO4可使溶液由Y点到X点 |
| D、在t℃时,以0.01molL-1AgNO3溶液滴定20mL O.01molL-1KC1和0.01molL-1的K2CrO4的混和溶液,CrO42-先沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CaO+H2O═Ca(OH)2 | ||||
| B、2Na2O2+2H2O═4NaOH+O2↑ | ||||
| C、2Na+2H2O═2NaOH+H2↑ | ||||
D、C+H2O
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 纯净物 | 混合物 | 强电解质 | 弱电解质 | 非电解质 | |
| A | 稀盐酸 | 水煤气 | 硫酸 | 醋酸 | 干冰 |
| B | 蒸馏水 | 蔗糖溶液 | 硫酸钡 | 一水合氨 | 二氧化硫 |
| C | 胆矾 | 稀硫酸 | 铁 | 水 | 碳酸钙 |
| D | 明矾 | 氢氧化铁胶体 | 氯化钠 | 次氯酸 | 氯气 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com