
| A. | 向卤代烃水解后的溶液中加入AaNO3溶液,根据沉淀颜色可以判断卤素原子种类 | |
| B. | 银镜反应、乙酸乙酯的水解反应、苯的硝化反应均需水浴加热 | |
| C. | 甲酸酯、葡萄糖、麦芽糖均能发生银镜反应 | |
| D. | 石油催化裂化的主要目的是提高汽油等轻质油的产量与质量;石油裂解的主要目的是为了得到更多的乙烯、丙烯等气态短链烃 |
分析 A.卤代烃在碱性条件下水解,直接加入硝酸银易生成氢氧化银沉淀;
B.银镜反应、乙酸乙酯的水解反应、苯的硝化反应需提供温度的稳定;
C.甲酸酯、葡萄糖、麦芽糖均含有醛基;
D.根据裂解和裂化的目的来分析.
解答 解:A.卤代烃在碱性条件下水解,直接加入硝酸银易生成氢氧化银沉淀,干扰实验结果,应加入酸酸化,故A错误;
B.学化学中需要水浴的实验有:银镜反应、蔗糖、纤维素、淀粉水解、苯的硝化、苯的磺化、酯类的水解等,故B正确;
C.甲酸酯、葡萄糖、麦芽糖均含有醛基,均能发生银镜反应,故C正确;
D.石油催化裂化的主要目的是提高汽油等轻质油的产量与质量;石油裂解的主要目的是得到更多的乙烯、丙烯等气态短链烃,故D正确.
故选A.
点评 本题多角度考查有机物的结构和性质,为高考常见题型,侧重学生的分析能力的考查,有利于双基的夯实,注意把握有机物的组成、结构和官能团的性质,难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇能够使蛋白质变性,75%(体积分数)的乙醇溶液可用于医疗消毒 | |
| B. | 乙二醇的水溶液凝固点很低,可用作汽车发动机的抗冻剂 | |
| C. | 光照时乙烷与氯气能发生取代反应,工业上常用该反应生产氯乙烷 | |
| D. | 油脂的碱性水解又称为皂化,其产物之一高级脂肪酸盐可用于制造肥皂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
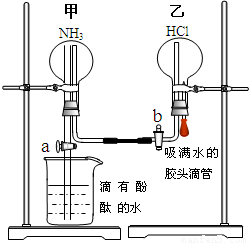 某探究学习小组的同学学习氨的性质以后,为了探究氨气的某些性质,设计并进行了以下实验:
某探究学习小组的同学学习氨的性质以后,为了探究氨气的某些性质,设计并进行了以下实验:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
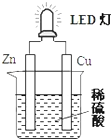
| A. | 铜片表面有气泡生成,锌片上发生氧化反应 | |
| B. | 如果将稀硫酸换成葡萄糖溶液,不能使LED灯发光 | |
| C. | 装置中存在“化学能→电能→光能”的转换 | |
| D. | 如果将铜片换成铁片,则锌片为正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al2O3既不是氧化剂也不是还原剂 | B. | 氧化剂与还原剂物质的量比是1:3 | ||
| C. | AlN是还原产物 | D. | 每生成1 mol AlN有2mol电子转移 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com