
【题目】K2Cr2O7溶液中存在平衡:Cr2O72-(橙色)+H2O![]() 2CrO42-(黄色)+2H+。用K2Cr2O7溶液进行下列实验:
2CrO42-(黄色)+2H+。用K2Cr2O7溶液进行下列实验:
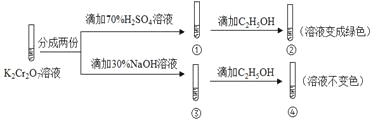
结合实验,下列说法不正确的是
A. ①中溶液橙色加深,③中溶液变黄
B. ②中Cr2O72-被C2H5OH还原
C. 对比②和④可知K2Cr2O7酸性溶液氧化性强
D. 若向④中加入70%H2SO4溶液至过量,溶液变为橙色
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】25℃时,在10 mL浓度均为0.1 mol/LNaOH和NH3·H2O混合溶液中滴加0.1 mol/L盐酸,下列有关溶液中粒子浓度关系正确的是( )
A.未加盐酸时:c(OH-)>c(Na+)=c(NH3·H2O)
B.加入盐酸至溶液pH=7时:c(Cl-)=c(Na+)
C.加入10 mL盐酸时:c(NH![]() )+c(H+)=c(OH-)
)+c(H+)=c(OH-)
D.加入20 mL盐酸时:c(Cl-)=c(NH![]() )+c(Na+)
)+c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 需要加热才能发生的反应一定是吸热反应
B. 由C(石墨,s)=C(金刚石,s) △H=+1.9kJ/mol,可知金刚石比石墨稳定
C. 自发反应的熵一定增大,非自发反应的熵一定减小
D. 等质量的硫蒸气和硫固体分别完全燃烧,前者放出的热量多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol·L-1的三种酸(HA、HB和HD)溶液,滴定的曲线如图所示,下列判断错误的是( )
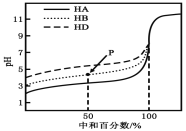
A.三种酸的电离常数关系:KHA>KHB>KHD
B.滴定至P点时,溶液中:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-)
C.pH=7时,三种溶液中:c(A-)=c(B-)=c(D-)
D.当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)=c(OH-)-c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将氯水分别滴入下列各选项所述的溶液中,由实验现象得出的结论完全正确的是( )
选项 | 氯水滴入下列溶液中 | 实验现象 | 结论 |
A | 滴有KSCN的FeCl2溶液 | 变红 | Cl2具有还原性 |
B | 滴有酚酞的NaOH溶液 | 褪色 | Cl2具有漂白性 |
C | 紫色石蕊溶液 | 先变红后褪色 | Cl2具有酸性、漂白性 |
D | KI淀粉溶液 | 变蓝色 | Cl2具有氧化性 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以某含铜矿石[主要成分是FeCuSi3O13(OH)4,含少量SiO2、CaCO3]为原料制备CuSO4·5H2O的流程如下:
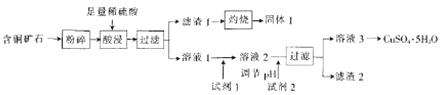
已知相关试剂成分和价格如下表所示:
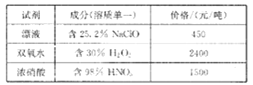
请回答下列问题:
(1)含铜矿石粉碎的目的是_______。
(2)酸浸后的溶液中除了Cu2+外,还含有的金属阳离子是_______。
(3)固体1溶于NaOH溶液的离子方程式为__________。
(4)结合题中信息可知:所选用的试剂1的名称为_______;加入该试剂时,发生反应的离子方程式为_________。
(5)试剂2 可以选择下列物成中的______。滤渣2中一定含有的物质为______(填化学式)。
A. Cu B.CuO C.Cu(OH)2 D.Fe
(6)CuSO4·5H2O用于电解精炼铜时,导线中通过9.632×103C的电量,测得阳极溶解的铜为16.0g。而电解质溶液(原溶液为1 L)中恰好无CuSO4,则理论上阴极质量增加_____g,原电解液中CuSO4的浓度为__ 。已知一个电子的电量为1.6×10-19C)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
a、b、c、d、e是原子序数依次递增的五种短周期元素,其中a元素组成的一种粒子不含电子;b元素的最高价氧化物的水化物甲能与其氢化物生成一种盐乙;d的单质能与酸、碱反应均生成氢气;a,b,d三种元素能与c元素形成常见的化合物;d,e两种元素组成de3型化合物.
(1)写出由以上某些元素构成的既含极性共价键,又含非极性共价键的化合物的电子式_________(写出一种即可)
(2)b的常见氢化物的空间构型是_________:b、c的最简单氢化物中稳定性最强的是_____(填化学式)。
(3)写出三种由以上元素组成的具有漂白性的物质_________(写化学式)。
(4)be3和含有ec2-离子的溶液反应可生成ec2气体和一种碱性气体,写出其离子方程式________.
(5)常温下,甲、乙的水溶液的 pH 均为 5。则两溶液中由水电离出的 H+浓度之比是_________.
(6)由上述元素所形成的常见物质 X、Y、Z、W、M、N 有如下转化关系:

①X 溶液与 Y 溶液反应的离子方程式为___________
②将一小块N的金属箔在酒精灯上加热至熔化后的现象为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com