
| A�� | ƽ��ǰ�����ŷ�Ӧ�Ľ��У�������ѹǿ��С | |
| B�� | ƽ��ʱ�������������䣬�����H2O��g�����淴Ӧ���ʼ�С | |
| C�� | ƽ��ʱ�������������䣬�����¶�ƽ�ⳣ������ | |
| D�� | �����������䣬ʹ�ò�ͬ������HCl��g����ת���ʲ��� |
���� �÷�Ӧ��һ����Ӧǰ�����������С�����ȵĿ��淴Ӧ���ڷ�Ӧ�ﵽƽ��֮ǰ�������������ѹǿ�ڲ��ϼ�С�������H2O��g��������С������Ũ�ȣ��淴Ӧ���ʼ�С�������¶�ƽ�����淴Ӧ�����ƶ���ƽ�ⳣ����С��ʹ�ô���ֻ�ı仯ѧ��Ӧ���ʵ���Ӱ��ƽ����ƶ���ת���ʲ��䣮
��� �⣺A���÷�Ӧ��һ����Ӧǰ�����������С�����ȵĿ��淴Ӧ���ڷ�Ӧ�ﵽƽ��֮ǰ�����ŷ�Ӧ�Ľ��У���������ʵ�����С����������ѹǿ����С����A��ȷ��
B�������H2O��g��������С������Ũ�ȣ��淴Ӧ���ʼ�С����B��ȷ��
C���÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ�������¶�ƽ�����淴Ӧ�����ƶ���ƽ�ⳣ����С����C����
D��ʹ�ô���ֻ�ı仯ѧ��Ӧ���ʵ���Ӱ��ƽ����ƶ���ת���ʲ��䣬��D��ȷ��
��ѡC��
���� ���⿼����Ӱ�컯ѧƽ������أ��ѶȲ���ע�����ֻӰ�췴Ӧ���ʲ�Ӱ��ƽ����ƶ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ѧ��Ӧ��ʵ���Ǿɻ�ѧ�����Ѻ��»�ѧ�����γ� | |
| B�� | �����ɸ������������ת��ʱ���ų����� | |
| C�� | ��һ��������Cȼ�գ�����CO2ʱ������COʱ�ų��������� | |
| D�� | �ɱ�����ʱ�ų��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | BF3 | B�� | BeCl2 | C�� | PC13 | D�� | SO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
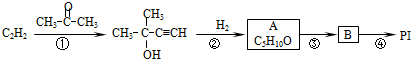
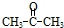 ����Ϊ����ȩ���������ڢۢܺ�õ�����Ľṹ��ʽ��
����Ϊ����ȩ���������ڢۢܺ�õ�����Ľṹ��ʽ��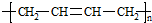 ��
��

 +n NaOH��
+n NaOH�� +n CH3COONa��
+n CH3COONa���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ٺ͢ڻ�Ϻ�c��H+��=c��CH3COO-��+c��OH-��+2c��SO42-�� | |
| B�� | �ٺ͢���Һ�У�c��Na+��=c��CH3COO-��+c��CH3COOH��=0.01mol•L-1 | |
| C�� | �ں͢ۻ����Һ�У�c��SO42-����c��NH4+����c��OH-����c��H+�� | |
| D�� | ������Һ��ϡ��100������ҺpH���ܣ��ۣ��٣��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | A | B | C | D |
| װ�� | 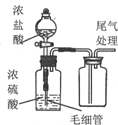 | 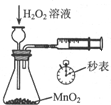 | 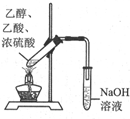 | 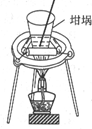 |
| Ŀ�� | ������ȡ����HCl���� | �ⶨ��ͬŨ�ȵ�H2O2��Һ�Բ���O2���ʵ�Ӱ�� | �Ʊ����ռ��������� | ��С�մ���Һ����ȡNaHCO3���� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
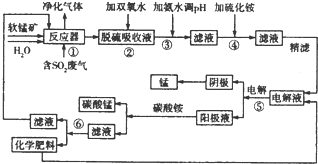
| ������ | Fe2+ | Fe3+ | Mn2+ | Ni2+ | Co2+ | |
| ����������� | ��ʼ������PH | 7.5 | 2.2 | 8.8 | 6.4 | 9.0 |
| ��ȫ������PH | 9.5 | 3.5 | 10.8 | 8.4 | ||
| ������� | ��ʼ������PH | 6.2 | 4.67 | |||
| ��ȫ������PH | ||||||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
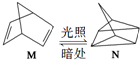 ��H=+88.6kJ•mol-1
��H=+88.6kJ•mol-1�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com