
科目:高中化学 来源: 题型:阅读理解
| ||
| ||
| 16m3 |
| m-m3 |
| 16m3 |
| m-m3 |
查看答案和解析>>
科目:高中化学 来源:活题巧解巧练·高考化学(第一轮) 题型:022
现在工业上主要采用离子交换膜电解食盐水制取H2,Cl2,NaOH.回答下列问题:
(1)在电解过程中,有电源正极相连的电极上所发生的电极反应式为________.
(2)电解之前食盐水需要精制,目的是除去粗盐中的Ca2+,Mg2+, 等杂质离子,实验的试剂有:a.Na2CO3溶液,b.Ba(OH)2溶液,c.稀盐酸,其合理的加入顺序为________(填试剂序号).
等杂质离子,实验的试剂有:a.Na2CO3溶液,b.Ba(OH)2溶液,c.稀盐酸,其合理的加入顺序为________(填试剂序号).
(3)如果在容积为10L的离子交换膜电解槽中,1min在阴极可产生11.2L(标准状况)Cl2,这时溶液的pH是(设体积维持不变)________.
(4)Cl2常用于自来水的消毒杀菌.现在有一种新型消毒剂ClO2,若它们在杀菌过程中的还原产物均为Cl-,消毒等量的自来水,所需Cl2和ClO2的物质的量之比为________.
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)在电解过程中,与电源正极相连的电极上所发生的电极反应式为_______________。
(2)电解之前食盐水需要精制,目的是除去粗盐中Ca2+、Mg2+、SO![]() 等杂质离子,使用的试剂有:a.Na2CO3溶液,b.Ba(OH)2溶液,c.稀盐酸,其合理的加入顺序为____________(填试剂序号)。
等杂质离子,使用的试剂有:a.Na2CO3溶液,b.Ba(OH)2溶液,c.稀盐酸,其合理的加入顺序为____________(填试剂序号)。
(3)如果在容积为10 L的离子交换膜电解槽中,1 min 在阴极可产生11.2 L(标准状况)Cl2,这时溶液的pH是(设体积维持不变)____________。
(4)Cl2常用于自来水的消毒杀菌,现有一种新型消毒剂ClO2,若它们在杀菌过程中的还原产物均为Cl-,消毒等量的自来水,所需Cl2和ClO2的物质的量之比为____________。
查看答案和解析>>
科目:高中化学 来源:2013届河北省五校联盟高三上学期调研考试理科综合化学试卷(带解析) 题型:实验题
【化学—选修2:化学与技术】(15分)
工业上采用电解饱和食盐水的方法生产烧碱和氯气。
Ⅰ.电解饱和食盐水之前,需精制食盐水。为了除去粗盐中的Ca2+、Mg2+、SO42-、及泥沙,可将粗盐溶于水,然后进行下列五项操作:①过滤;②加过量NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液。正确的操作顺序是 。
| A.④②①⑤③ | B.④①②⑤③ | C.②⑤④①③ |
| D.②④⑤①③ E.⑤②④①③ F.⑤④②①③ |
查看答案和解析>>
科目:高中化学 来源:2013届河北省五校联盟高三上学期调研考试理科综合化学试卷(解析版) 题型:实验题
【化学—选修2:化学与技术】(15分)
工业上采用电解饱和食盐水的方法生产烧碱和氯气。
Ⅰ.电解饱和食盐水之前,需精制食盐水。为了除去粗盐中的Ca2+、Mg2+、SO42-、及泥沙,可将粗盐溶于水,然后进行下列五项操作:①过滤;②加过量NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液。正确的操作顺序是 。
A.④②①⑤③ B.④①②⑤③ C.②⑤④①③
D.②④⑤①③ E.⑤②④①③ F.⑤④②①③
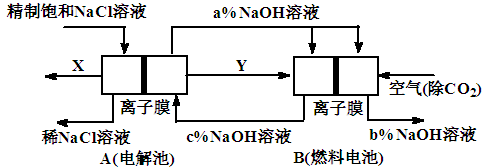
Ⅱ.氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。

⑴图中X、Y分别是_____、______(填化学式)
⑵分别写出燃料电池B中正极、负极上发生的电极反应
正极:___________ __; 负极:___________ ____;
⑶为什么必须将空气中的二氧化碳除去才能通入燃料电池? 。
⑷分析比较图示中氢氧化钠质量分数a%、b%和c%的大小 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com