
【题目】氯酸钾和浓盐酸之间有下列反应:2KClO3 + 4HCl(浓)== 2 KCl + Cl2↑+ 2ClO2 + 2H2O。
(1)该反应中发生还原反应的物质是__________。氧化产物是___________。
(2)用双线桥标出方程式中的电子得失___________。
2KClO3 + 4HCl(浓)== 2 KCl + Cl2↑+ 2ClO2 + 2H2O
(3)当有0.2mol电子发生转移时,生成的氯气的体积为_____L(标准状况)。被氧化的HCl的物质的量为____mol。
(4)若分别用①KMnO4(还原产物是Mn2+)②MnO2(还原产物是Mn2+)③Ca(ClO)2(还原产物是Cl2)氧化浓盐酸制备氯气,当浓盐酸足量且这三种氧化剂的物质的量相同时,生成氯气的物质的量最少的是________。
【答案】 KClO3 Cl2 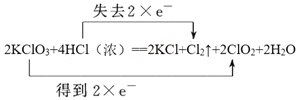 2.24 0.2 ②
2.24 0.2 ②
【解析】(1)氯酸钾中氯元素化合价从+5价降低到+4价,得到1个电子,因此该反应中发生还原反应的物质是KClO3。氯化氢中氯元素化合价从-1价升高到0价,失去电子,则氧化产物是Cl2。(2)根据以上分析可知用双线桥标出方程式中的电子得失为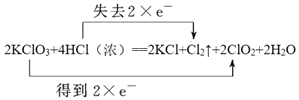 。(3)当有0.2mol电子发生转移时,生成的氯气是0.1mol,在标准状况下的体积为2.24L。根据氯原子守恒可知被氧化的HCl的物质的量为0.2mol。(4)假设均是1mol氧化剂参加反应,根据电子得失守恒可知1mol高锰酸钾得到氯气的物质的量是2.5mol,1mol二氧化锰得到氯气的物质的量是1mol,根据方程式Ca(ClO)2+4HCl=2Cl2↑+CaCl2+2H2O可知1mol次氯酸钙得到2mol氯气,所以生成氯气的物质的量最少的是二氧化锰,答案选②。
。(3)当有0.2mol电子发生转移时,生成的氯气是0.1mol,在标准状况下的体积为2.24L。根据氯原子守恒可知被氧化的HCl的物质的量为0.2mol。(4)假设均是1mol氧化剂参加反应,根据电子得失守恒可知1mol高锰酸钾得到氯气的物质的量是2.5mol,1mol二氧化锰得到氯气的物质的量是1mol,根据方程式Ca(ClO)2+4HCl=2Cl2↑+CaCl2+2H2O可知1mol次氯酸钙得到2mol氯气,所以生成氯气的物质的量最少的是二氧化锰,答案选②。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】(1)可逆反应N2(g)+3H2(g)![]() 2NH3(g)是一个放热反应,有甲乙两个完全相同的容器,向甲容器中加入1 mol N2和3 mol H2在一定条件下,达到平衡时放出的热量为Q1,相同条件下,向乙容器中加入2 mol NH3,达到平衡时,吸收的热量为Q2,已知Q2=4Q1,则甲容器中H2的转化率为 。
2NH3(g)是一个放热反应,有甲乙两个完全相同的容器,向甲容器中加入1 mol N2和3 mol H2在一定条件下,达到平衡时放出的热量为Q1,相同条件下,向乙容器中加入2 mol NH3,达到平衡时,吸收的热量为Q2,已知Q2=4Q1,则甲容器中H2的转化率为 。
(2)除电解法,工业炼镁还可采用硅热法(Pidgeon法)。即以煅白(CaO·MgO)为原料与硅铁(含硅75%的硅铁合金)混合置于密闭还原炉,1200℃下发生反应:
2(CaO·MgO)(s) + Si(s) ![]() Ca2SiO4 (l) + 2Mg(g)
Ca2SiO4 (l) + 2Mg(g)
①已知还原性:Mg > Si,上述反应仍能发生的原因是______________________________
②由下图,推测上述反应正向为______(填“吸热”或“放热”)反应;平衡后若其他条件不变,将还原炉体积缩小一半,则达到新平衡时Mg(g)的浓度将______(填“升高”“降低”或“不变”)。

③若还原炉容积为400 m3,原料中煅白质量为9.6 t,5小时后,测得煅白的转化率为50%,
计算这段时间Mg的生成速率 _________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是高中阶段学习的常见单质或化合物,单质A在单质B中燃烧产生苍白色的火焰,产物溶于水得到常见的强酸。化合物C具有强氧化性、漂白性,是单质B与水反应的产物之一。化合物D是淡黄色物质,可用于呼吸面具,可由一种活泼金属E在氧气中燃烧得到。回答问题:
(1)物质C的名称____________ ,化合物D中非金属元素的化合价为___________。
(2)单质A在单质B中燃烧的化学方程式为___________。
(3)单质B与水反应的离子方程式为___________。
(4)化合物D与水反应的离子方程式___________。
(5)活泼金属E与水的反应中,单质E是______(填“氧化剂”或“还原剂”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下,溶液中能发生如下反应:①2R-+Z2===R2+2Z- ②16H++10Z-+2XO![]() ===2X2++5Z2+8H2O ③2M2++R2===2M3++2R-。由此判断,下列说法中正确的是( )
===2X2++5Z2+8H2O ③2M2++R2===2M3++2R-。由此判断,下列说法中正确的是( )
A. Z2+2M2+===2M3++2Z-不可以进行
B. Z元素在①②反应中都发生还原反应
C. X2+是还原剂XO4—的还原产物
D. 各粒子氧化性由强到弱的顺序是XO![]() >Z2>R2>M3+
>Z2>R2>M3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Cl-、Br-、Fe2+、I-的还原性依次增强。现向FeBr2、FeI2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如下图所示,请回答:

(1)c线分别代表溶液中____________的变化情况;
(2)原溶液中Fe2+与Br-的物质的量之比为____________;
(3)当通入2mol Cl2时,溶液中离子反应为__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】巴豆酸的结构简式为CH3—CH=CH—COOH,现有①氯化氢②溴水③纯碱溶液④乙醇⑤酸性高锰酸钾溶液,根据巴豆酸的结构特点,判断在一定条件下,能与巴豆酸反应的物质是
A. 只有②④⑤ B. 只有①③④ C. 只有①②③⑤ D. ①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W均为短周期主族元素,它们在周期表中相对位置如图所示。Z和Y两元素可以形成常见ZY3型化合物,下列说法正确的是

A. X的常见氢化物比Y的常见氢化物稳定
B. X、Z、W的氧化物对应水化物都是常见的强酸
C. W单质不能从盐溶液中置换出Z单质
D. X、Z均可与Y形成原子个数比为1:2的共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“富勒烯”家族又增添了新成员,继C60、C70、N60之后,科学家首次发现了全硼富勒烯B40 。下列说法正确的是( )
A. B40、C70都属于新型化合物 B. B40、C60、C70、N60都只含非极性共价键
C. B40、C60、C70、N60都属于烯烃 D. C60和N60属于同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在下列物质中:①Cu ②CuSO4固体③CO ④干冰 ⑤FeCl3溶液 ⑥蔗糖溶液 ⑦熔融MgSO4 ⑧硫磺(请用序号填空)。属于电解质的是__________________。
(2)CO2是形成温室效应的罪魁祸首。
①CO2的摩尔质量为_________g/mol;
②44 g CO2的物质的量为________mol,在标准状况下的体积约为_______L。
(3)同温同压下,同体积O2和O3的质量比____,同质量O2和O3所含氧原子的个数比为____。
(4)在一定的温度和压强下,1体积X2 (气)跟3体积Y2 (气)化合生成2体积化合物,则该化合物的化学式是_____________。
(5)三种正盐的混合溶液中含有0.2 mol Na+、0.25 mol Mg2+、0.4 mol Cl-、SO42-,则SO42-物质的量为___________mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com