
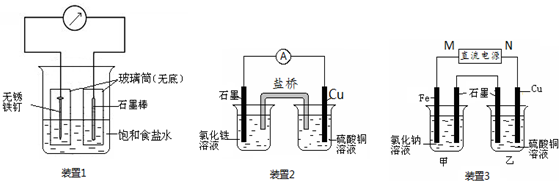
分析 (1)铁发生吸氧腐蚀,铁被氧化生成Fe2+,Fe2+与K3[Fe(CN)6]反应生成蓝色沉淀,正极发生还原反应,氧气得到电子被还原生成OH-;
(2)形成原电池,总方程式为Cu+2Fe3+=Cu2++2Fe2+,根据总方程式判断;
(3)向甲烧杯中滴入几滴酚酞,观察到石墨电极附近首先变红,说明石墨极生成4OH-,应为电解池的阴极,则铁为阳极,则M为正极,N为负极,乙烧杯为电解硫酸的反应,阳极生成氧气,阴极析出铜,结合电极方程式解答该题.
解答 解:(1)铁发生吸氧腐蚀,铁被氧化生成Fe2+,正极发生还原反应,氧气得到电子被还原生成OH-,电极方程式为O2+4e-+2H2O-═4OH-,
故答案为:氧化;O2+4e-+2H2O-═4OH-;
(2)铜可被Fe3++氧化,发生Cu+2Fe3+=Cu2++2Fe2+,形成原电池反应时,铜为负极,发生氧化反应,石墨为正极,正极反应为Fe3++e-=Fe2+,
故答案为:正; Cu+2Fe3+=Cu2++2Fe2+;
(3)装置3中甲烧杯盛放100mL 0.2mol/L的NaCl溶液,乙烧杯盛放100mL 0.5mol/L的CuSO4溶液.反应一段时间后,停止通电.向甲烧杯中滴入几滴酚酞,观察到石墨电极附近首先变红,故甲池中石墨极为阴极,则铁极为阳极,乙池中铜做阴极,石墨做阳极.
①向甲烧杯中滴入几滴酚酞,观察到石墨电极附近首先变红,说明石墨极生成4OH-,应为电解池的阴极,则铁为阳极,电极反应为 Fe-2e-═Fe2+,则M为正极,
故答案为:正;Fe-2e-═Fe2+;
②乙烧杯中用铁做阴极、石墨做阳极来电解硫酸铜溶液,阳极上氢氧根放电生成氧气,阴极上铜离子放电析出铜,电解方程式为2Cu2++2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+4H+,
故答案为:2Cu2++2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+4H+;
③取出Cu电极,洗涤、干燥、称量、电极增重0.64g,则生成Cu的物质的量为$\frac{0.64g}{64g/mol}$=0.01mol,转移的电子的物质的量为0.01mol×2=0.02mol,
甲烧杯中,阳极铁被氧化,阴极产生气体为氢气,
2H2O+2e-═2OH-+H2↑,
2mol 22.4L
0.02mol V
V=$\frac{22.4L×0.02mol}{2mol}$=0.224L,即224mL.
故答案为:224.
点评 本题考查电化学知识,题目难度中等,做题时注意电极的判断和电极反应的书写,注意串联电路中各电极转移的电子数目相等,利用反应的方程式计算.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
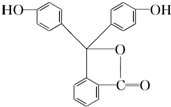 酚酞是中学化学中常用的酸碱指示剂,其结构如下,完成下列问题:
酚酞是中学化学中常用的酸碱指示剂,其结构如下,完成下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 阳离子 | K+、Na+、Al3+、Cu2+ |
| 阴离子 | OH-、HCO3-、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤干馏后的产物可以制造氮肥 | |
| B. | 可在周期表的过渡元素中寻找半导体材料 | |
| C. | 可用新制的氢氧化铜检验葡萄糖 | |
| D. | 可用氯气制备漂白粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 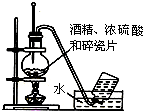 实验室用乙醇制取乙烯 | B. | 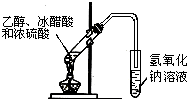 实验室制取乙酸乙酯 | ||
| C. |  分离苯和甲苯 | D. |  实验室制取硝基苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a 或b | B. | c | C. | d 或e | D. | f |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com