
常温下体积相同的下列四种溶液:①pH=3的盐酸②pH=3的醋酸溶液③pH=11的氨水④pH=11的NaOH溶液.下列说法中,正确的是()
A. ②和④混合,所得混合溶液的pH大于7
B. 将四种溶液分别稀释到体积为原的100倍,溶液pH大小顺序③>④>②>①
C. ③和④分别与足量稀硫酸中和,消耗硫酸的体积③=④
D. ①和③混合,所得混合溶液中c(H+)+c(NH4+)=c(Cl﹣)+c(OH﹣)
考点: 酸碱混合时的定性判断及有关ph的计算.
专题: 电离平衡与溶液的pH专题.
分析: pH=3的CH3COOH溶液中c(CH3COOH)>10﹣3mol/L,pH=3的盐酸中c(HCl)=10﹣3mol/L,pH=11的氨水中c(NH3.H2O)>10﹣3mol/L,pH=11的NaOH溶液中c(NaOH)=10﹣3mol/L,
A.②和④等体积混合后,醋酸过量,溶液显示酸性;
B.醋酸和氨水为弱酸、弱碱,稀释过程中电离程度增大;盐酸和氢氧化钠分别为强酸、强碱,稀释后溶液的pH分别变为5、9;
C.根据碱的物质的量浓度大小确定消耗硫酸的体积;
D.根据混合液中一定满足电荷守恒进行判断.
解答: 解:pH=3的CH3COOH溶液中c(CH3COOH)>10﹣3 mol/L,pH=3的盐酸中c(HCl)=10﹣3 mol/L,pH=11的氨水中c(NH3.H2O)>10﹣3mol/L,pH=11的NaOH溶液中c(NaOH)=10﹣3 mol/L,
A.②和④混合,醋酸浓度大于氢氧化钠溶液,所以二者混合后溶液显示酸性,溶液的pH<7,故A错误;
B.醋酸稀释稀释过程中溶液中氢离子的物质的量增大,则醋酸稀释100倍后溶液的3<pH<5;氨水稀释后溶液中氢氧根离子物质的量增大,则氨水稀释100倍后溶液的9<pH<11;盐酸稀释100倍后溶液的pH=5、氢氧化钠溶液稀释100倍后溶液的pH=9,所以将四种溶液分别稀释到体积为原的100倍,溶液pH大小顺序为:③>④>①>②,故B错误;
C.由于c(NH3.H2O)>c(NaOH),所以等体积的③和④分别用等浓度的硫酸溶液中和,消耗硫酸溶液的体积:③>④,故C错误;
D.①盐酸和③氨水混合,所得混合溶液中一定满足电荷守恒:c(H+)+c(NH4+)=c(Cl﹣)+c(OH﹣),故D正确;
故选D.
点评: 本题考查酸碱混合溶液的定性判断,注意掌握酸碱混合后的定性判断及溶液酸碱性与溶液pH的关系,明确强弱电解质的特点是解本题关键,题目难度中等.


科目:高中化学 来源: 题型:
(1)NH3经一系列反应可以得到HNO3和NH4NO3,如图所示,在Ⅰ中,NH3和O2在催化剂作用下反应,其化学方程式是 .
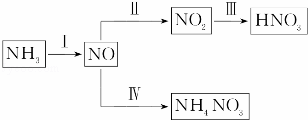
(2)Ⅱ中,2NO(g)+O2(g)⇌2NO2(g).在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下温度变化的曲线(如图).
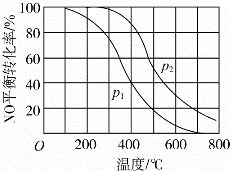
①p1、p2的大小关系 .
②随温度升高,该反应平衡常数变化的趋势是
(3)Ⅲ中,降低温度,将NO2(g)转化为N2O4(1)再制备浓硝酸.
①已知:2NO2(g)⇌N2O4(g)△H1 2NO2(g)⇌N2O4(1)△H2
下列能量变化示意图3中,正确的是A(选填字母)
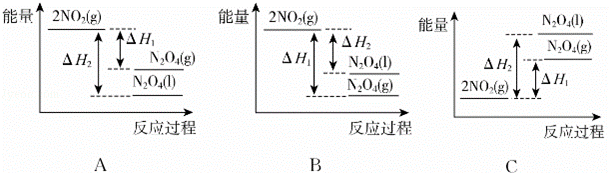
②N2O4与O2,H2O化合的化学方程式是
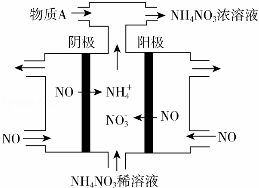
(4)Ⅳ中,电解NO制备NH4NO3,其原理原理如图4所示,为使电解产物全部转化为NH4NO3,需补充物质A,A是NH3,说明理由: .
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应aA(s)+bB(g)⇌cC(g)+dD(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是()
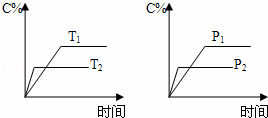
A. 达到平衡后,加入催化剂则C%增大
B. 达到平衡后,若升高温度,平衡向左移动
C. 化学方程式中b>c+d
D. 达平衡后,增加A的量,有利于平衡向右移动
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,向a L密闭容器中加入1mol X气体和2mol Y气体,发生如下反应:X(g)+2Y(g)⇌2Z(g),此反应达到平衡的标志是()
A. 容器内压强不随时间变化
B. v正(X)=v逆(Z)
C. 容器内X、Y、Z的浓度之比为1:2:2
D. 单位时间消耗0.1molX同时生成0.2molZ
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,一定浓度的某溶液,由水电离出的c(OH﹣﹣)=10﹣﹣4mol/L,则该溶液中的溶质可能是()
A. Na2SO4 B. CH3COOH C. NaOH D. CH3COOK
查看答案和解析>>
科目:高中化学 来源: 题型:
对于2SO2(g)+O2(g)⇌2SO3(g)△H<0 反应来说:
(1)若将2mol SO2气体和1mol O2气体在2L容器中混合并在一定条件下发生反应,经2min建立平衡,此时测得SO3浓度为0.8mol•L﹣1,则从开始至2min用氧气表示的平均速率v(O2)= ;该条件时反应的平衡常数K= .
(2)在体积不变的条件下,改变下列条件重新达到平衡时能使平衡常数K增大的有 (填字母).
A.升高温度B.降低温度C.增大压强 D.移出生成的SO3
(3)一定温度下,若将8mol SO2气体和4mol O2气体混合置于体积恒定的密闭容器中,能说明该反应已达到平衡状态的是 .
A.SO2的转化率和O2的转化率相等 B.容器内压强保持不变
C.v(SO2)逆=2v(O2)正 D.容器内密度保持不变
(4)一定温度下,将8mol SO2和4mol O2气体混合置于体积不变的密闭容器中,经t1时间达到平衡,测得混合气体总物质的量为10mol.若此时向容器中充入一定量的氦气,SO3(g)的物质的量将不变(填“增大”、“减小”或“不变”);若使SO2、O2、SO3三种气体均增加1mol,则平衡 (填“向左移动”、“向右移动”或“不移动”).
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物X催化氧化的产物是(CH3)2CHCHO,有机物X是( )
A. 乙醇的同系物 B. 乙醛的同系物
C. 丙醇的同分异构体 D. 丙醛的同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
硼和镁形成的化合物刷新了金属化合物超导温度的最高记录.如图是该化合物的晶体结构单元:镁原子间形成正六棱柱,且棱柱的上下面还各有一个镁原子;6个硼原子位于棱柱的侧棱上,则该化合物的化学式可表示为( )
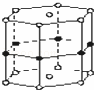
A. MgB B. Mg3B2 C. MgB2 D. Mg2B3
查看答案和解析>>
科目:高中化学 来源: 题型:
按图的装置进行电解,A极是铜锌含金,B极为纯铜.电解质溶液中含有足量的Cu2+.通电一段时间后,若A极恰好全部溶解,此时B极质量增加7.68g,溶液质量增加0.03g,则A极合金中Cu、Zn的原子个数比为()
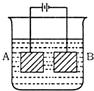
A. 4:1 B. 3:1 C. 2:1 D. 5:3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com