
【题目】可逆反应达到最大反应限度的本质特征是( )
A.正反应不再继续进行
B.正反应和逆反应都再继续进行
C.正反应和逆反应的速率都为零
D.正反应和逆反应的速率相等
 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源: 题型:
【题目】实验是学习化学的一个重要途径。
(1)图1是实验室常用的制气装置,其中b可用于制取O2和NH3,实验室用装置b制取NH3反应的化学方程式为______________________________________。若用二氧化锰和浓盐酸制取氯气应选择的装置为_______,反应的离子方程式为_____________________________。

(2)图2是实验室制备氯气并进行一系列相关实验的装置。
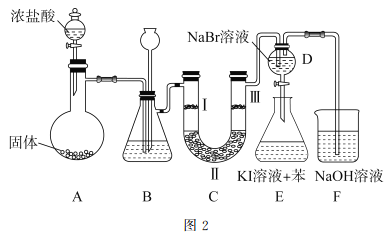
①装置B中盛装的液体试剂为_________。
②装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、II处依次放入的物质正确的是_________(填字母编号)。
编号 | I | II | III |
A | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
b | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
D | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
③D中发生反应的离子方程式是_________。将装置D中的溶液加入装置E中,溶液分为两层,上层呈紫红色,要分离出紫红色溶液,需使用的玻璃仪器是玻璃棒、烧杯和________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去下列物质内所含的杂质(括号内的物质),所选用的试剂不正确的是 ( )
A.乙酸(苯甲酸):NaOH溶液B.甲烷(乙烯):溴水
C.苯(苯甲酸):NaOH溶液D.乙炔(硫化氢):亚硫酸钠酸性溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组向某2 L密闭容器中加入一定量的固体A和气体B,发生反应
A(s)+2B(g) ![]() D(g)+E(g) ΔH=Q kJ·mol-1。在T1 ℃时,反应进行到不同时间测得各物质的物质的量如表:
D(g)+E(g) ΔH=Q kJ·mol-1。在T1 ℃时,反应进行到不同时间测得各物质的物质的量如表:
时间(min) 物质的量(mol) | 0 | 10 | 20 | 30 | 40 | 50 |
B | 2.00 | 1.36 | 1.00 | 1.00 | 1.20 | 1.20 |
D | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |
E | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |
(1)T 1 ℃时,该反应的平衡常数K=________。
(2)30 min后,只改变某一条件,反应重新达到平衡,根据表中的数据判断改变的条件可能是________(填字母编号)。
a.通入一定量的B
b.加入一定量的固体A
c.适当缩小容器的体积
d.升高反应体系温度
e.同时加入0.2 mol B、0.1 mol D、0.1 mol E
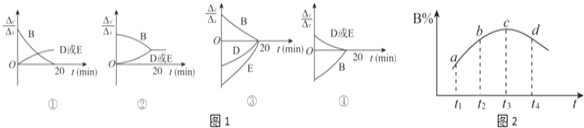
(3)对于该反应,用各物质表示的反应速率与时间的关系示意曲线为图1中的________(填序号)。
(4)维持容器的体积和温度T1 ℃不变,若向该容器中加入1.60 mol B、0.20 mol D、0.20 mol E和n mol A,达到平衡后,与表格中20分钟时各物质的浓度完全相同,则投入固体A的物质的量n的取值范围是________。
(5)维持容器的体积和温度T1 ℃不变,各物质的起始物质的量为:n(A)=1.0 mol,n(B)=3.0 mol,n(D)=a mol,n(E)=0 mol,达到平衡后,n(E)=0.50 mol,则a=________。
(6)若该密闭容器绝热,实验测得B的转化率B% 随温度变化的示意图如图2所示。由图可知,Q_______0(填“大于”或“小于”),c点v正_______v逆(填“大于”、“小于”或“等于”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列信息判断氢气燃烧生成水时的热量变化,其中一定正确的是( )

A. H2O分解为H2与O2时放出热量
B. 生成1mol H2O时吸收热量245 kJ
C. 甲、乙、丙中物质所具有的总能量大小关系为乙>甲>丙
D. 氢气和氧气的总能量小于水的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量的水后,产生1.16g白色沉淀。再向所得悬浊液中逐滴加入1.00mol/L HCl溶液,加入HCl溶液的体积与生成沉淀的关系如图所示。试回答:
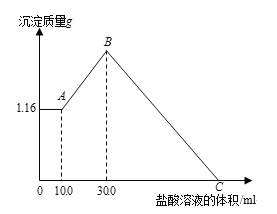
(1)写出A点到B点发生反应的离子方程式
(2)C点加入盐酸溶液的体积为 。
(3)原混合物中MgCl2的物质的量是 ,NaOH的质量是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是( )
A. 若在海轮外壳上附着一些铜块,则可以减缓海轮外壳的腐蚀
B. 2NO(g)+2CO(g)===N2(g)+2CO2(g)在常温下能自发进行,则该反应的ΔH>0
C. 加热0.1 mol·L-1Na2CO3溶液,CO![]() 的水解程度和溶液的pH均增大
的水解程度和溶液的pH均增大
D. 对于乙酸与乙醇的酯化反应(ΔH<0),加入少量浓硫酸并加热,该反应的反应速率和平衡常数均增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示,其中NH3被氧化为常见的无毒物质。下列说法错误的是( )

A. 溶液中OH-向电极a移动
B. 电极b上发生还原反应
C. 负极的电极反应为2NH3-6e-+6OH-![]() N2+6H2O
N2+6H2O
D. 理论反应消耗的NH3与O2的物质的量之比为3:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃煤和汽车尾气是造成空气污染的原因之一,雾疆天气肆虐给人类健康带来了严重影响,化学在解决雾霾污染中发挥了重要作用。
(1)煤燃烧产生的烟气中含有氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
己知:
CH4(g)+2NO2(g) ![]() N2(g)+CO2(g)+2H2O(g) △H=-867 kJ·mol-1
N2(g)+CO2(g)+2H2O(g) △H=-867 kJ·mol-1
2NO2(g) ![]() N2O4(g) △H=-56.9kJ·mol-1
N2O4(g) △H=-56.9kJ·mol-1
H2O(g)=H2O(l) △H=-44.0kJ·mol-1
①写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式________________。
②反应CH4(g)+2NO2(g) ![]() N2(g)+CO2(g)+2H2O(l)在恒温恒容容器中达到平衡,下列叙述不能作为判断该反应达到平衡状态标志的是___________。
N2(g)+CO2(g)+2H2O(l)在恒温恒容容器中达到平衡,下列叙述不能作为判断该反应达到平衡状态标志的是___________。
A.容器中的压强不变 B.混合气体的密度不变
C.2v正(NO2)= v 逆(N2) D.c(CH4)= c(N2)
(2)CO、CO2 是火力发电厂及汽车尾气的主要成分,为减少对环境造成的影响,采用以下方法将其资源化利用。
①以CO 为电极燃料,以熔融K2CO3为电解质,和O2组成燃料电池。请写出该电池的负极电极反应式_____________________。
②在铝矾土作催化剂、773K条件下,3molCO与1.5molSO2反应生成3molCO2和0.75mol硫蒸气,该反应可用于从烟道气中回收硫,写出该反应的化学方程式_______________。
③在汽车的排气管上增加一个补燃器,并不断补充O2使其浓度保持为4.0×10-4mol·L-1,发生反应2CO(g)+O2(g) ![]() 2CO2(g)。某温度下测得汽车尾气中CO、CO2 气体的浓度分别为2.0×10-6 mol·L-1、4.0×10-4 mol·L-1,则该条件下反应的平衡常数K=___________。
2CO2(g)。某温度下测得汽车尾气中CO、CO2 气体的浓度分别为2.0×10-6 mol·L-1、4.0×10-4 mol·L-1,则该条件下反应的平衡常数K=___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com