
 将一定质量的镁、铝合金投入100mL一定物质的量浓度HCl中,合金全部溶解,向所得溶液中滴加5mol/LNaOH溶液到过量,
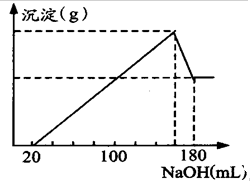
将一定质量的镁、铝合金投入100mL一定物质的量浓度HCl中,合金全部溶解,向所得溶液中滴加5mol/LNaOH溶液到过量,分析 (1)由图可知,从开始至加入NaOH溶液20mL,没有沉淀生成,说明原溶液中盐酸溶解Mg、Al后有剩余,此时发生的反应为:HCl+NaOH=NaCl+H2O.继续滴加NaOH溶液,到沉淀量最大,此时为Mg(OH)2和Al(OH)3,二者质量之和为19.4g,溶液为氯化钠溶液.再继续滴加NaOH溶液,到沉淀量开始进行,到沉淀量最小时,沉淀为Mg(OH)2,质量为11.6g,故到沉淀量最大,Al(OH)3的质量为19.4g-11.6g=7.8g,
由元素守恒可知,n(Al)=n[Al(OH)3],n(Mg)=n[Mg(OH)2],再利用m=nM计算Al、Mg的质量;
(2)加入20mLNaOH溶液,恰好中和剩余的盐酸,此时溶液中溶质为AlCl3、MgCl2、NaCl,根据氯元素守恒有n(HCl)=3n(AlCl3)+2n(MgCl2)+n(NaCl),根据钠元素守恒此时溶液中n(NaCl)=n(NaOH),据此计算出n(HCl),再利用c=$\frac{n}{V}$计算盐酸的物质的量浓度.
解答 解:(1)由图可知,从开始至加入NaOH溶液20mL,没有沉淀生成,说明原溶液中盐酸溶解Mg、Al后有剩余,此时发生的反应为:HCl+NaOH=NaCl+H2O.继续滴加NaOH溶液,到沉淀量最大,此时为Mg(OH)2和Al(OH)3,二者质量之和为19.4g,溶液为氯化钠溶液.再继续滴加NaOH溶液,到沉淀量开始进行,到沉淀量最小时,沉淀为Mg(OH)2,质量为11.6g,故到沉淀量最大,Al(OH)3的质量为19.4g-11.6g=7.8g.
由元素守恒可知,n(Al)=n[Al(OH)3]=$\frac{7.8g}{78g/mol}$=0.1mol,所以m(Al)=0.1mol×27g/mol=2.7g,
n(Mg)=n[Mg(OH)2]=$\frac{11.6g}{58g/mol}$=0.2mol,所以m(Mg)=0.2mol×24g/mol=4.8g,
答:原合金中Mg、A1质量分别为m(Mg)=4.8g,m(Al)=2.7g;
(2)加入20mLNaOH溶液,恰好中和剩余的盐酸,此时溶液中溶质为AlCl3、MgCl2、NaCl,根据氯元素守恒有n(HCl)=3n(AlCl3)+2n(MgCl2)+n(NaCl),根据钠元素守恒此时溶液中n(NaCl)=n(NaOH)=0.02L×5mol/L=0.1mol,所以n(HCl)=3n(AlCl3)+2n(MgCl2)+n(NaCl)=3×0.1mol+2×0.2mol+0.1mol=0.8mol,原盐酸的物质的量浓度为$\frac{0.8mol}{0.1L}$=8mol/L.
答:盐酸的物质的量浓度为8mol/L.
点评 本题考查镁铝化合物性质、混合物的计算,以图象题的形式考查,题目难度中等,分析图象各阶段的发生的反应是解题关键,再利用守恒计算,试题培养了学生的化学计算能力.


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 7.8 g Na2O2与足量潮湿的CO2反应,转移的电子数为0.1 NA | |
| B. | 标准状况下2.24 L HCHO中含0.4 NA个原子 | |
| C. | 23.4g NaCl晶体中含0.1 NA个如图所示结构单元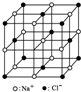 | |
| D. | 4.0gSiC晶体中含有的共价键数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验步骤 | 预期现象或结论 |
| 步骤1:取少量固体样品溶于无氧蒸馏水中 | 固体完全溶解得无色澄清溶液 |
| 步骤2:加入过量盐酸 | |
| 步骤3:静置后取上清液,加入BaCl2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 64gCaC2晶体中阴离子数目是2NA | |
| B. | 36g冰晶体中氢键数目是4NA | |
| C. | pH=13的NaOH溶液中阴阳离子总数目为0.2NA | |
| D. | 1L0.1mol•L-1FeCl3溶液中Fe3+水解产生的H+数目为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 误食重金属盐可立即喝鲜牛奶或鸡蛋清解毒 | |
| B. | 硅是人类将太阳能转换为电能的常用材料 | |
| C. | Al(OH)3可用来治疗胃酸过多,其原因是发生了氧化还原反应 | |
| D. | 高铁酸钾(K2FeO4)是新型高效多功能水处理剂,既能消毒杀菌又能净水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.8g水所含有的电子数目为NA | |
| B. | 等物质的量的CaCO3和KHCO3的质量均为100g | |
| C. | 11.2L氧气所含分子数目为0.5NA | |
| D. | 200mL 0.5mol/L Na2SO4溶液所含Na+数目0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH溶液(Ba(OH)2):用K2SO4溶液 | B. | NaCl溶液(Na2SO4):用Ba(NO3)2溶液 | ||
| C. | KOH溶液K2CO3:用CaCl2溶液 | D. | HNO3溶液(HCl):用AgNO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 合金的硬度往往大于它的纯金属 | B. | 合金的熔点高于它的成分金属 | ||
| C. | 青铜是我国使用最早的合金 | D. | 钢是使用量最大,用途最广的合金 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com