纳米级Cu
2O由于具有优良的催化性能而受到关注,如表为制取Cu
2O的三种方法:
| 方法Ⅰ | 用炭粉在高温条件下还原CuO |
| 方法Ⅱ | 电解法:2Cu+H2O Cu2O+H2↑ |
| 方法Ⅲ | 用肼(N2H4)还原新制Cu(OH)2 |
(1)工业上常用方法Ⅱ和方法Ⅲ制取Cu
2O而很少用方法Ⅰ,其原因是反应条件不易控制,若控温不当易生成
而使Cu
2O产率降低.
(2)已知:①C(s)+O
2(g)=CO
2(g)△H=akJ?mol
-1;
②2CO(g)+O
2(g)=2CO
2(g)△H=bkJ?mol
-1;
③2Cu
2O(s)+O
2(g)=4CuO(s)△H=ckJ?mol
-1.
方法Ⅰ制备过程会产生有毒气体,写出制备反应的热化学方程式
.
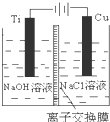
(3)方法Ⅱ采用离子交换膜
控制电解液中OH
-的浓度而制备纳米Cu
2O,装置如图所示,该电池的阳极生成Cu
2O反应式为
.
(4)方法Ⅲ为加热条件下用液态肼(N
2H
4)还原新制Cu(OH)
2来制备纳米级Cu
2O,同时放出N
2.该制法的化学方程式为
.
(5)方法Ⅲ可以用甲醛稀溶液替代肼,但因反应温度较高而使部分产品颗粒过大,
(填操作名称)可分离出颗粒过大的Cu
2O
(6)在相同的密闭容器中,用方法Ⅱ和方法Ⅲ制得的Cu
2O分别进行催化分解水的实验:
2H
2O(g)
2H
2(g)+O
2△H>0
水蒸气的浓度(mol?L
-1)随时间t (min)变化如表:
| 序号 | 温度 | 0 | 10 | 20 | 30 | 40 | 50 |
| ① | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
| ② | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
| ③ | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
可以判断:实验①的前20min的平均反应速率 ν(O
2)=
;实验温度T
1
T
2(填“>”、“<”);催化剂的催化效率:实验①
实验②(填“>”、“<”).

 纳米级Cu2O由于具有优良的催化性能而受到关注,如表为制取Cu2O的三种方法:
纳米级Cu2O由于具有优良的催化性能而受到关注,如表为制取Cu2O的三种方法: