
【题目】某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验.请回答下列问题: 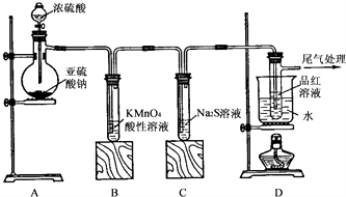
(1)装置A中盛放浓硫酸的仪器名称是;
(2)实验过程中,装置B中发生的现象是 , 说明 SO2具有性;装置C中发生的现象是 , 说明 SO2具有性;
(3)装置D的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象:;
(4)尾气可采用溶液吸收,反应方程式为 .
【答案】
(1)分液漏斗
(2)紫色褪去;还原;无色溶液中出现黄色浑浊;氧化
(3)品红溶液褪色后,关闭分液漏斗的旋塞,点燃酒精灯加热,溶液恢复为红色
(4)NaOH;SO2+2NaOH=Na2SO3+H2O
【解析】解:(1.)装置A中盛放浓硫酸的仪器是分液漏斗,所以答案是:分液漏斗;
(2.)二氧化硫和高锰酸钾溶液发生氧化还原反应生成硫酸,高锰酸钾被还原生成锰离子,二氧化硫能和硫化氢发生反应生成淡黄色沉淀,所以C中出现黄色浑浊,该反应中,二氧化硫中的硫元素化合价由+4价变为0价,所以二氧化硫得电子而作氧化剂,体现氧化性,所以答案是:紫色褪去;还原;无色溶液中出现黄色浑浊;氧化;
(3.)二氧化硫能和有色物质反应生成无色物质,所以二氧化硫能使品红溶液褪色,但二氧化硫的漂白性不稳定,加热无色溶液时,溶液又变为红色,其操作方法和现象为:品红溶液褪色后,关闭分液漏斗的旋塞,点燃酒精灯加热,溶液恢复为红色,所以答案是:品红溶液褪色后,关闭分液漏斗的旋塞,;
(4.)二氧化硫属于酸性氧化物,能和碱反应生成盐和水,所以能用碱液氢氧化钠溶液吸收,离子反应方程式为:SO2+2NaOH=Na2SO3+H2O,所以答案是:NaOH;SO2+2NaOH=Na2SO3+H2O.


科目:高中化学 来源: 题型:
【题目】化合物H是一种有机光电材料中间体.实验室由芳香化合物A制备H的一种合成路线如下: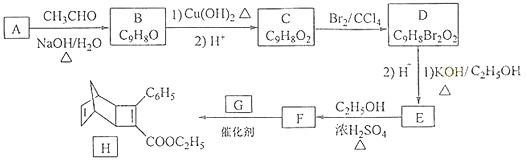
已知:①RCHO+CH3CHO ![]() RCH=CHCHO+H2O
RCH=CHCHO+H2O
② ![]() +
+ ![]()
![]()
![]()
回答下列问题:
(1)A的化学名称为为 .
(2)由C生成D和E生成F的反应类型分别为、 .
(3)E的结构简式为 .
(4)G为甲苯的同分异构体,由F生成H的化学方程式为 .
(5)芳香化合物X是F的同分异构体,X能与饱和碳酸氢钠溶液反应放出CO2 , 其核磁共振氢谱显示有4种不同化学环境的氢,峰面积比为6:2:1:1,写出2种符合要求的X的结构简式 .
(6)写出用环戊烷和2﹣丁炔为原料制备化合物 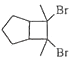 的合成路线(其他试剂任选).
的合成路线(其他试剂任选).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年8月5日在巴西里约召开的第31届奥运会,由于兴奋剂事件而使多名俄罗斯运动员遭到禁赛,禁止运动员使用兴奋剂是奥运会公平、公正的重要举措之一.以下有两种兴奋剂的结构分别为: 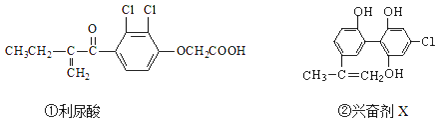
则关于以上两种兴奋剂的说法中不正确的是( )
A.利尿酸能发生取代反应、加成反应和酯化反应
B.1mol兴奋剂X与足量浓溴水反应,最多消耗3molBr2
C.可用FeCl3溶液检测利尿酸中是否含有兴奋剂X
D.1mol兴奋剂X最多都能和5molNaOH的溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的类别和核心元素的化合价是研究物质性质的两个重要角度。请根据下图所示,回答下列问题:
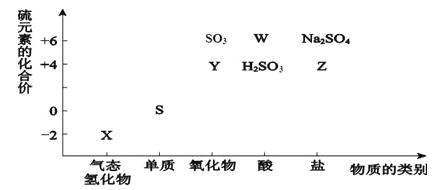
(1)X的化学式为__________,Y的化学式为__________。
(2)W的浓溶液与铜单质在加热条件下可以发生化学反应,反应的化学方程式为_________。
(3)欲制备Na2S2O3,从氧化还原角度分析,合理的是________(填序号)。
A.Na2S + S B.Na2SO3 + S C.Na2SO3 + Na2SO4 D.SO2 + Na2SO4
(4)将X与SO2混合,可生成淡黄色固体。该反应的氧化产物与还原产物的质量之比为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各选项有机物数目,与分子式为ClC4H7O2且能与碳酸氢钠反应生成气体的有机物数目相同的是(不含立体异构)( )
A.分子式为C5H10 的烯烃
B.分子式为C4H8O2 的酯
C.甲苯( ![]() )的一氯代物
)的一氯代物
D.立体烷( ![]() )的二氯代物
)的二氯代物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质不能按![]() “
“![]() ” 表示反应一步完成关系转化的是
” 表示反应一步完成关系转化的是 ![]()
选项 | a | b | c |
A | SiO2 | Na2SiO3 | H2SiO3 |
B | AlCl3 | Al(OH)3 | NaAlO2 |
C | Fe | Fe(OH)3 | Fe2O3 |
D | MgCl2 | Mg(OH)2 | MgO |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应2A(g)+B(g) ![]() 2C(g),若2 s(秒)后测得C的浓度为0.6 mol/L,现有下列几种说法:
2C(g),若2 s(秒)后测得C的浓度为0.6 mol/L,现有下列几种说法:
①用物质A表示反应的平均速率为0.3 mol/(L·s)
②用物质B表示反应的平均速率为0.6 mol/(L·s)
③2 s时物质A的转化率为70%
④2 s时物质B的浓度为0.7 mol/L
其中正确的是( )
A.①③
B.①④
C.②③
D.③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com