
有人建议用AG表示溶液酸度,AG定义为 AG=lg[c(H+)/c(OH-)]。回答下列问题:
(1)25℃时,溶液的AG与其pH之间的关系为AG= 。
(2)25℃时,一元弱碱MOH溶液的AG=-8。取20mL该MOH溶液,当与16.2mL 0.05 mol/L硫酸混合时,两者恰好完全中和。求此条件下该一元弱碱的电离平衡常数。
(1)AG = 2×(7-pH) (2)1.25×10-5 mol/L
【解析】
试题分析:(1)pH=-lgc(H+).25℃时AG=lg[c(H+)/c(OH-)]=lg c(H+)-lg c(OH-)= lg c(H+)-lg 10-14/c(H+)= 2lg c(H+)+14=2×(7-pH)。(2)MOH溶液的AG=-8,则pH=11.c(OH-)=10-3mol/L二者发生反应的方程式为2MOH+H2SO4=M2SO4+2H2O。n(H2SO4) = 0.0162L ×0.05 mol/L=8.1×10-4mol.所以c(MOH)= (2×8.1×10-4mol)÷0.02L=0.081mol/L.因此该一元弱碱的电离平衡常数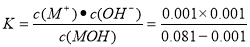 =1.25×10-5 mol/L
=1.25×10-5 mol/L
考点:考查AG与其pH之间的关系、弱电解质的大量平衡常数的计算的知识。


科目:高中化学 来源:2016届天津市五区县高一上学期期末考试化学试卷(解析版) 题型:选择题
下列关于物质用途的叙述中,错误的是 ( )
A.明矾溶于水形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化
B.用氧化铝坩埚加热熔化氢氧化钠固体
C.二氧化硅可以用于制造光导纤维
D.硅用作太阳能电池材料
查看答案和解析>>
科目:高中化学 来源:2016届吉林省高一上学期期末质量检测化学试卷(解析版) 题型:选择题
对I~IV的实验操作现象判断正确的是
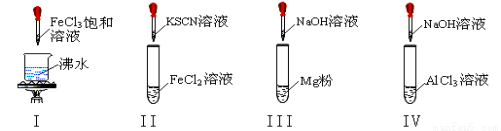
A.实验I:产生红褐色沉淀 B.实验II:溶液颜色变红
C.实验III:放出大量气体 D.实验IV:先出现白色沉淀,后溶解
查看答案和解析>>
科目:高中化学 来源:2016届云南省高一下学期第一次月考化学试卷(解析版) 题型:选择题
某电荷数小于18的元素X,其原子核外电子层数为a,最外层电子数为(2a+1)。下列有关元素X的说法中,不正确的是 ( )
A.元素X的原子核内质子数为(2a2-1)
B.元素X形成的单质既能作氧化剂又能作还原剂
C.元素X形成的简单离子,各电子层的电子数均达到2n2个(n表示电子层数)
D.由元素X形成的某些化合物,可能具有杀菌消毒的作用
查看答案和解析>>
科目:高中化学 来源:2016届云南省高一下学期第一次月考化学试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.1.0 mol·L-1KNO3溶液:H+,Fe2+,Cl-,SO42-
B.石蕊溶液呈红色的溶液:NH4+,Ba2+,AlO2-,Cl—
C.与铝反应产生大量氢气的溶液:Na+,K+,NH4+,NO3-
D.pH=12的溶液:K+,Na+,NO3—,Cl—
查看答案和解析>>
科目:高中化学 来源:2015届福建省龙岩市高二第一学期教学质量检测化学试卷(解析版) 题型:填空题
工业上常常利用反应①来生产环氧乙烷,但是伴随副反应②。
①C2H4(g)+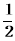 O2(g) →
O2(g) →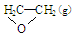 ; △H1 ②C2H4(g)+3O2(g) → 2CO2(g)+2H2O(g); △H2
; △H1 ②C2H4(g)+3O2(g) → 2CO2(g)+2H2O(g); △H2
(1)写出环氧乙烷充分燃烧的热化学反应方程式。答:____________________________;
(2)工业生产中,可通过某一措施来加快反应①而对反应②影响较小,从而提高环氧乙烷的生产效率。工业生产采取的这种措施是_______________。
A.升高反应体系的温度B.增大体系中氧气的浓度
C.使用合适的催化剂D.降低反应体系的压强
(3)已知C=C、O=O、C—C键能分别为a kJ·mol-1、b kJ·mol-1、c kJ·mol-1,则环氧乙烷中C—O键能为 kJ·mol-1;
(4)反应②可以设计成燃料电池,若以酸做电解质溶液,负极反应式是 。
查看答案和解析>>
科目:高中化学 来源:2015届福建省龙岩市高二第一学期教学质量检测化学试卷(解析版) 题型:选择题
如图为某种甲醇燃料电池示意图,工作时电子流方向如图所示。下列判断正确的是
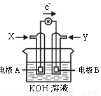
A. X为氧气
B.电极A反应式:CH3OH-6e-+H2O = CO2+6H+
C. B电极附近溶液pH增大
D.电极材料活泼性:A>B
查看答案和解析>>
科目:高中化学 来源:2015届福建省四地六校高二下学期第一次月考化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.蛋白质、淀粉、纤维素和油脂都是高分子有机物
B.苯和乙酸乙酯都能发生取代反应
C.煤干馏可得苯及甲苯等,是由于煤中含有苯及甲苯等物质
D.淀粉、纤维素和蛋白质水解都生成葡萄糖
查看答案和解析>>
科目:高中化学 来源:2015届湖北省黄石市高二上学期期末考试化学试卷(解析版) 题型:选择题
在密闭容器中,使2 mol N2和6 mol H2混合发生下列反应:N2(g)+3H2(g)  2NH3(g)(正反应为放热反应)。下列说法错误的是
2NH3(g)(正反应为放热反应)。下列说法错误的是
A.升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量变大
B.升高平衡体系的温度(保持体积不变),混合气体的密度不变
C.当反应达到平衡时,N2和H2的浓度比是 1∶3
D.当达到平衡时,充入氩气,并保持压强不变,平衡将逆向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com