
| |||||||||||||||||||||||||||
科目:高中化学 来源: 题型:阅读理解
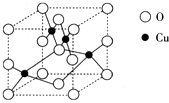 (2009?广东)铜单质及其化合物在很多领域有重要的用途,如金属铜用来制造电线电缆,五水硫酸铜可用作杀菌剂.
(2009?广东)铜单质及其化合物在很多领域有重要的用途,如金属铜用来制造电线电缆,五水硫酸铜可用作杀菌剂.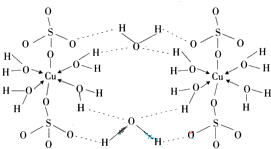
查看答案和解析>>
科目:高中化学 来源: 题型:
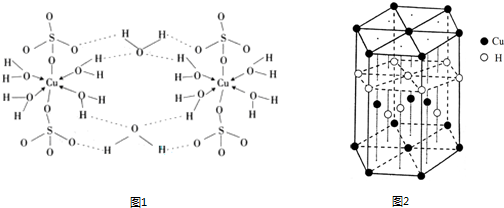
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

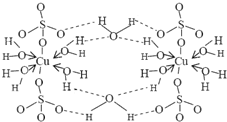


查看答案和解析>>
科目:高中化学 来源: 题型:
| A、称取12.5g胆矾(CuSO4?5 H2O),溶于500mL水配成溶液 | B、称取12.0g胆矾(CuSO4?5 H2O),配成500mL溶液 | C、称取1.0g CuSO4,配成500mL溶液 | D、称取12.5g胆矾(CuSO4?5 H2O),配成500mL溶液 |
查看答案和解析>>
科目:高中化学 来源:导学大课堂必修一化学人教版 人教版 题型:022
下列10种物质:①水 ②空气 ③铁 ④二氧化碳 ⑤硫酸 ⑥熟石灰(Ca(OH)2) ⑦胆矾(CuSO4·5 H2O) ⑧Fe(OH)3胶体 ⑨碱式碳酸铜(Cu2(OH)2CO3) ⑩硫酸氢钠(NaHSO4)中,属于混合物的是________;属于氧化物的是________;属于碱的是________;属于酸的是________;属于盐的是________.(以上空格填物质的序号)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com