
| A. | 原子序数为15的元素的最高化合价为+3 | |
| B. | ⅦA族元素是同周期中非金属性最强的元素 | |
| C. | 原子序数为12的元素位于元素周期表的第三周期ⅡA族 | |
| D. | 第二周期ⅣA族元素的原子核电荷数和中子数一定为6 |
分析 A.原子序数为15的元素为P,最外层有5个电子;
B..ⅦA族元素位于周期表的右侧,同周期从左向右非金属性增强;
C.原子序数为12的元素原子核外有3个电子层,最外层电子数为2;
D.第二周期ⅣA族元素为C,质子数=核电荷数=6,但中子数不确定.
解答 解:A.原子序数为15的元素为P,最外层有5个电子,元素的最高化合价为+5,故A错误;
B..ⅦA族元素位于周期表的右侧,同周期从左向右非金属性增强,则ⅦA族元素是同周期中非金属性最强的元素,故B正确;
C.原子序数为12的元素原子核外有3个电子层,最外层电子数为2,位于元素周期表的第三周期ⅡA族,故C正确;
D.第二周期ⅣA族元素为C,质子数=核电荷数=6,但中子数不确定,中子数可能为6、7、8,故D错误.
故选BC.
点评 本题考查元素周期表的结构及应用,为高频考点,把握周期表中原子序数及元素的位置、元素周期律的应用为解答的关键,侧重基础知识的考查,题目难度不大.


 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 甲烷和氯气可以发生取代反应 | B. | 乙烯和高锰酸钾可以发生加成反应 | ||
| C. | 酯化反应中醇脱羟基酸脱氢 | D. | 乙醇可以发生银镜反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X与Y只能形成一种化合物 | |
| B. | 最高价氧化物对应水化物的碱性:Y>Z | |
| C. | 单质熔点:M<N | |
| D. | 单质的氧化性:X<M |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl和NaOH反应的中和热△H=-57.3 kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ/mol | |
| B. | CO(g)的燃烧热△H=-283.0 kJ/mol,则2CO2(g)═2CO(g)+O2(g)反应的△H=+2×283.0 kJ/mol | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | 1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 肯定没有SO2和NO | B. | 肯定没有Cl2、O2和NO2 | ||
| C. | 可能有Cl2和O2 | D. | 肯定只有NO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性 | |
| B. | 浓硝酸在光照下颜色变黄,说明浓硝酸不稳定 | |
| C. | 常温下,浓硝酸可以用铝罐贮存,说明铝与浓硝酸不反应 | |
| D. | 氨水可使酚酞试剂变为红色,说明氨溶解于水显弱碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 非电解质:乙醇、氯气 | B. | 酸性氧化物:NO、SO2 | ||
| C. | 碱:烧碱、纯碱 | D. | 混合物:铝热剂、盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
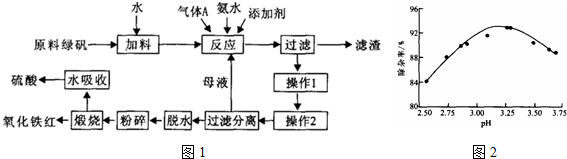
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com