
| A. | 防止催化剂中毒 | B. | 提高反应效率 | C. | 提高SO2转化率 | D. | 防止环境污染 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液氨常被用作制冷剂 | |
| B. | 可利用2Fe3++Cu═Cu2++2Fe2+腐蚀印刷电路板 | |
| C. | 为便于储存和使用,可用液氯代替氯水漂白干燥棉布上的有色物质 | |
| D. | 已知3Cl2+8NH3═N2+6NH4Cl,工业上可用浓氨水检查氯气管道是否漏气 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.15mol/L | B. | 0.10mol/L | C. | 0.25mol/L | D. | 0.40mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
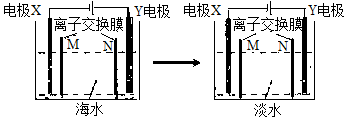
| A. | N是阴离子交换膜 | B. | Y电极上产生有色气体 | ||
| C. | X电极区域有浑浊产生 | D. | X电极反应式为4OH--4e-=O2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验事实 | 结论 |
| A | 向纯碱中滴加足量浓盐酸,将产生的气体通入硅酸钠溶液,溶液变浑浊 | 酸性:盐酸>碳酸>硅酸 |
| B | 向某溶液中加入2滴KSCN溶液,溶液不显红色.再向溶液中加入几滴新制的氯水,溶液变为红色 | 该溶液中一定含有Fe2+ |
| C | SiO2可以和NaOH溶液及HF溶液反应 | SiO2属于两性氧化物 |
| D | 取某溶液少量,加入盐酸酸化的氯化钡溶液,出现白色沉淀 | 该溶液中一定含有大量的SO42- |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com