
| A、CH4、C2H2、C2H4 |
| B、C2H6、C3H6、C4H6 |
| C、CH4、C3H8、C2H6 |
| D、C2H2、C2H4、C2H6 |
| y |
| 4 |
| y |
| 2 |
| y |
| 4 |
| y |
| 2 |
| y |
| 4 |
| y |
| 4 |
| y |
| 4 |


科目:高中化学 来源: 题型:
| A、由Fe、Cu、FeCl3溶液组成原电池,负极反应式为:Cu-2e-=Cu2+ |
| B、由Al、Cu、稀硫酸组成原电池,负极反应式为:Cu-2e-=Cu2+ |
| C、由Al、Mg、NaOH溶液组成原电池,负极反应式为:Al+4OH--3e-=AlO2-+2H2O |
| D、由Al、Cu、浓硝酸组成的原电池中,负极反应式为:Al-3e-=Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②③④ | B、①③ |
| C、①②④ | D、①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、M>N>P>Z |
| B、M>N>Z>P |
| C、Z>P>M>N |
| D、P>M>N>Z |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H>-820 kJ?mol-1 |
| B、CH4的燃烧热是820kJ?mol-1 |
| C、1mol CH4和2mol O2的键能之和大于1mol CO2和2mol H2O的键能之和 |
| D、11.2L(标准状况)CH4完全燃烧生成气态水时放出410kJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | A | B | C | D |
| 装置或操作 |  |
 |
 |
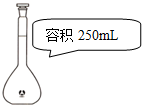 |
| 实验目的 | 石油的蒸馏 | 除去Cl2中的HCl | 存放液溴 | 配制240mL 0.1mol/L的NaCl溶液 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:

 表示氢原子,
表示氢原子, 表示氧原子,它们组成的分子发生了如图所示的反应.关于该反应的说法不正确的是( )
表示氧原子,它们组成的分子发生了如图所示的反应.关于该反应的说法不正确的是( )| A、该反应属于化合反应 |
| B、反应前后元素种类没有改变 |
| C、原子在化学反应中不能再分 |
| D、反应前后分子的种类没有改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、25℃时,pH=13的1.0L Ba(OH)2溶液中含有的OH-数目为0.2NA |
| B、1 mol OH-在电解过程中完全放电时电路中通过了NA个电子 |
| C、铜的电解精炼时,阳极上每转移2mol电子时就溶解铜原子NA个 |
| D、1mol/L的Na2CO3溶液中CO32-粒子数目小于NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
 肼(N2H4)广泛用于火箭推进剂、有机合成及电池燃料.请回答下列问题:
肼(N2H4)广泛用于火箭推进剂、有机合成及电池燃料.请回答下列问题:| 实验Ⅰ:催化剂用量与配比对催化 活性影响 |
实验Ⅱ:水合肼用量对反应时间的影响 | 实验Ⅲ:反应温度对反应时间的影响 | ||||||||
| 序号 | m(Fe3+) /g |
m(Al3+) /g |
100%转化 消耗时间/min |
序号 | n(对氯硝基苯):n(水合肼) | 反应时间/min | 序号 | 反应温度/℃ | 反应时间/min | 转化率% |
| ① | 5 | 5 | 70 | ① | 1:1.5 | 110 | ① | 78 | 70 | 89 |
| ② | 10 | 不加 | 110 | ② | 1:1.8 | 110 | ② | 75 | 60 | 91 |
| ③ | 10 | 0.8 | 60 | ③ | 1:2.0 | 40 | ③ | 70 | 40 | 100 |
| ④ | 10 | 1 | 40 | ④ | 1:2.2 | 30 | ④ | 65 | 110 | 95 |
| ⑤ | 20 | 1 | 70 | / | / | / | ⑤ | 60 | 110 | 88 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com