
| A. | ④③②① | B. | ④③①② | C. | ③④①② | D. | ①③④② |
分析 Na与溶液反应实质上是和溶液的氢离子的反应,所以氢离子浓度越大,反应越剧烈,依题意,直接比较物质的氢离子浓度.
解答 解:Na与溶液反应实质上是和溶液的氢离子的反应,所以氢离子浓度越大,反应越剧烈;
盐酸为酸,本身电离产生大量氢离子,0.5mol•L-1盐酸氢离子浓度为0.5mol/L;氯化铁为强酸弱碱盐,水解生成氢离子,但是水解是微弱的,0.1mol•L-1FeCl3溶液中氢离子浓度小于0.1mol•L-1;水为弱电解质,电离产生氢离子浓度等于10-7mol/L;乙醇非电解质,溶液中氢离子浓度为0;
氢离子浓度越大,反应越剧烈,所以反应的剧烈程度由强到弱的是③④①②,
故选:C.
点评 本题考查了反应速率快慢的比较,明确钠的性质是解题关键,注意溶液中离子浓度大小比较方法,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | BaSO3与稀HNO3反应:3BaSO3+2H++2NO3-═3BaSO4+2NO↑+H2O | |
| B. | 碳酸钠溶液中滴加少量氯水的离子方程式为:CO32-+Cl2+H2O=HCO3-+Cl-+HClO | |
| C. | Fe2(SO4)3溶液与Ba(OH)2溶液反应:Fe3++SO42-+Ba2++3OH-═Fe(OH)3↓+BaSO4↓ | |
| D. | 向FeI2溶液中滴加少量氯水,反应的离子方程式为:2Fe2++Cl2═2Fe3++2Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
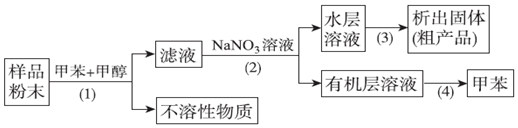
| A. | 步骤(1)需要过滤装置 | |
| B. | 步骤(3)需要用到蒸发皿 | |
| C. | 活性天然产物易溶于有机溶剂难溶于水 | |
| D. | 步骤(4)是利用物质沸点差异进行分离的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 过量的Fe粉中加入稀HNO3,充分反应后,滴入KSCN溶液 | 溶液呈红色 | 稀HNO3将Fe氧化为Fe3+ |
| B | 两试管各加入5ml 0.1mol/L Na2S2O3溶液,同时分别滴入5ml 0.1mol/L硫酸和盐酸 | 两支试管同时变浑浊 | 其它条件不变时,Cl-一定有催化效果 |
| C | A1箔插入稀HNO3中 | 无现象 | A1箔表面被HNO3氧化,形成致密的氧化膜 |
| D | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | V(N2)=0.01mol/(L•S) | B. | V(H2)=0.2mol/(L•S) | ||
| C. | V(H2)=0.6mol/(L•min) | D. | V(NH3)=1.2mol/(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸氢钠溶液中加稀盐酸入:HCO3-+H+═CO2↑+H2O | |
| B. | 碳酸钡和稀硝酸反应:CO32-+2H+═CO2↑+H2O | |
| C. | 铜片插入硝酸银溶液:Cu+Ag+═Cu2++Ag | |
| D. | 把金属铁放入稀硫酸中:2Fe+6H+═2Fe3++3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 放电时:电子移动方向由Pb通过导线向PbO2传递 | |
| B. | 充电时:阳极反应是PbSO42-+2e-+2H2O═PbO2+SO42-+4H+ | |
| C. | 放电时:正极反应是Pb-2e-+SO42-═PbSO4 | |
| D. | 充电时:铅蓄电池的阴极应与电源的正极相连 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 绿色化学的核心是在化学合成中将原子充分利用,转化为新的原子 | |
| B. | 研发使用高效催化剂,可提高反应中原料的转化率 | |
| C. | 高纯度的晶体桂可以制备晶体管等半导体、电脑芯片 | |
| D. | 酒精、NaCl溶液、CuSO4溶液、浓HNO3都可使蛋白质发生变性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在常温常压下,2.24L NH3与1.8g H2O,所含的质子数均为NA | |
| B. | 在常温常压下,1mol Cl2与足量的NaOH溶液完全反应,转移电子2NA | |
| C. | 在标准状况下,64g SO2 中含有的原子数为3NA | |
| D. | 在标准状况下,11.2L H2O含有的分子数为0.5NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com