
| A. | 等物质的量浓度的(NH4)2CO3溶液和(NH4)2SO4溶液中c(NH4+)相同 | |
| B. | FeCl3溶液不能与固体CaCO3发生反应 | |
| C. | 一定条件下,反应2Mg(s)+CO2(g)═C(s)+2MgO(s)具有自发性,其△H>0 | |
| D. | 将0.005mol Na2O2溶于水得到1L溶液,此溶液在常温下的pH=12 |
分析 A.相同系数的铵盐溶液,根据溶液中其它离子是促进铵根离子水解还是抑制铵根离子水解判断c(NH4+)大小;
B.FeCl3溶液呈酸性,能溶解碳酸钙;
C.根据△G=△H-T•△S判断;
D.将0.005mol Na2O2溶于水得到1L溶液,此溶液溶质为0.01mol NaOH,根据KW、PH=-lgC(H+)计算.
解答 解:A.(NH4)2CO3 中NH4+水解显酸性,CO32-水解显碱性,两者相互促进,所以NH4+水解的量较多,NH4+的量较少,(NH4)2SO4中硫酸根离子对铵根离子浓度无影响,即溶液中c(NH4+),(NH4)2SO4>(NH4)2CO3,故A错误;
B.Fe3+易水解,水解生成H+,水解的离子方程式为Fe3++3H2O?Fe(OH)3+3H+,能与固体CaCO3发生反应生成二氧化碳气体,故B错误;
C.一定条件下,反应2Mg(s)+CO2(g)═C(s)+2MgO(s),该反应的△S<0,若具有自发性,则应符合△G=△H-T△S<0,则△H<0,故C错误;
D.Na2O2溶于水,反应生成氢氧化钠和氧气,离子反应为2Na2O2+2H2O=4Na++4OH-+O2↑,将0.005mol Na2O2溶于水得到1L溶液,此溶液溶质为0.01mol NaOH,常温下水的离子积为1×10-14,则该溶液中氢离子浓度为:$\frac{1×1{0}^{-14}}{0.01}$=10-12,所以该溶液的pH=-lgc(H+)=12,
故选D.
点评 本题考查盐类水解、反应进行的方向、溶液的PH计算等,题目难度中等,注意反应能否自发进行的判断方法,学习中深刻理解相关概念,为易错点.


 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案科目:高中化学 来源: 题型:选择题
| A. | 研究采煤、采油新技术,提高产量以满足工业生产的快速发展 | |
| B. | 加大开发太阳能、水能、风能、地热能等能源力度,减少化石燃料的使用 | |
| C. | 研制推广以乙醇为燃料的汽车或大力推广电动汽车 | |
| D. | 生产、生活中,努力实现资源的循环利用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丁烷是直链烃,是因为分子中4个碳原子在同一条直线上 | |
| B. | 丙烷的一氯代物有2种,丙烷的二氯代物有4种 | |
| C. | 丙烯中所有原子均在同一平面上 | |
| D. | 甲苯上的某一个氢原子被-C3H7取代后,所得有机产物有6种 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | HCl和F2 | B. | NO和CO | C. | NH2-和NH4+ | D. | CH4和H2S |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 用下图装置可以测定混合气体中ClO2的含量
用下图装置可以测定混合气体中ClO2的含量查看答案和解析>>
科目:高中化学 来源: 题型:解答题
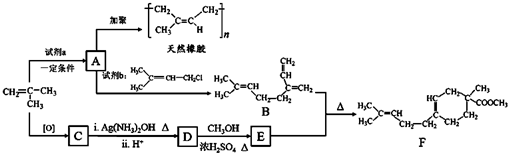
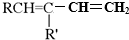
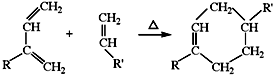 (R、R′可以是氢原子、烃基或官能团)
(R、R′可以是氢原子、烃基或官能团) .
.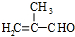 .
.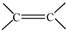 和
和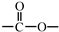 结构的D的所有同分异构共有7种(不包括顺反异构体),写出其中任意两种的结构简式CH2=CHCH2COOH、CH2=CHCOOCH3等.
结构的D的所有同分异构共有7种(不包括顺反异构体),写出其中任意两种的结构简式CH2=CHCH2COOH、CH2=CHCOOCH3等.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 密度不变 | B. | 温度不变 | C. | 颜色不变 | D. | 压强不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 若气体是H2,则原溶液中还可能大量存在:NH4+、CO32-、SO42- | |
| B. | 若气体是H2,则原溶液中还可能大量存在:Ba2+、Cl-、NO3- | |
| C. | 若气体是NO,则原溶液中还可能大量存在:NH4+、Fe3+、SO42- | |
| D. | 若气体是NO,则原溶液中还可能大量存在:K+、Na+、SO32- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com