
����Ŀ��������Ϊ���ڱ��еĵ�VA��Ԫ�أ����ǵ�Ԫ�ؼ��仯�����������ϼ������������в�ͬ�ԡ��ش��������⣺
��1��N2����������Nԭ�Ӷ��ﵽ8�����ȶ�״̬��������Nԭ��֮�乲�е��ӵ���ĿΪ____________�����ķ���ʽΪP4,4��Pԭ���֮�乲�γ�6�����۵�������ÿ��Pԭ�Ӷ��ﵽ8�����ȶ�״̬��������ӵĿռ乹��Ϊ____________��
��2��N��P����Ԫ�ض����γɶ�����̬�⻯�������N2H4)Ϊ��Ԫ�����ˮ�еĵ����백���ƣ�д��������ˮ�е�һ�����뷽��ʽ___________________________�����������ᣨH3PO4���γɵ���������εĻ�ѧ����ʽΪ_________________________________��
��3��P2O5��һ�ָ�������������岻����P2O5�������________������ĸ��ţ���
A.SO2 B.NH3 C.CO D.H2 E.H2S F.O2
��4�������ᣨH3PO2����һԪ��ǿ�ᣬ���Ĺ�ҵ�Ʒ��ǽ�������Ba(OH)2��Һ��Ӧ����PH3�����Ba(H2PO2)2,��������H2SO4��Ӧ��д��������Ba(OH)2��Һ��Ӧ�Ļ�ѧ����ʽ________��Ba(H2PO2)2Ϊ_______________������Ρ�����ʽ�Ρ�)��
���𰸡� 6 �������� N2H4+H2O![]() N2H5++OH- N2H4+ 2H3PO4= N2H6(H2PO4)2 B 2P4+3Ba(OH)2+6H2O=3Ba(H2PO2)2+2PH3�� ����
N2H5++OH- N2H4+ 2H3PO4= N2H6(H2PO4)2 B 2P4+3Ba(OH)2+6H2O=3Ba(H2PO2)2+2PH3�� ����
����������1��N2����������Nԭ�Ӷ��ﵽ8�����ȶ�״̬��������ԭ�Ӽ��γ���3�Թ��õ��Ӷԣ�������Nԭ��֮�乲�е��ӵ���ĿΪ6�����ķ���ʽΪP4��4��Pԭ���֮�乲�γ�6�����۵�������ÿ��Pԭ�Ӷ��ﵽ8�����ȶ�״̬��������ӵĿռ乹��Ϊ����������
��2��N��P����Ԫ�ض����γɶ�����̬�⻯�������N2H4)Ϊ��Ԫ�����ˮ�еĵ����백���ƣ�������ˮ�е�һ�����뷽��ʽΪN2H4+H2O![]() N2H5++OH-�����������ᣨH3PO4���γɵ���������εĻ�ѧ����ʽΪN2H4+ 2H3PO4= N2H6 (H2PO4)2��
N2H5++OH-�����������ᣨH3PO4���γɵ���������εĻ�ѧ����ʽΪN2H4+ 2H3PO4= N2H6 (H2PO4)2��
��3��P2O5��һ�ָ�����������ܸ���ˮ��Һ�ʼ��Ե����壬������P2O5������ǰ�����ѡB ��
��4��������Ĺ�ҵ�Ʒ��ǽ�������Ba(OH)2��Һ��Ӧ����PH3�����Ba(H2PO2)2,��������H2SO4��Ӧ��������Ba(OH)2��Һ��Ӧ�Ļ�ѧ����ʽΪ2P4+3Ba(OH)2+6H2O=3Ba(H2PO2)2+2PH3������Ϊ�����ᣨH3PO2����һԪ��������Ba(H2PO2)2Ϊ������


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС��Ϊ̽��Ũ��������ʣ����������ͼ��ʾ��װ�ý���ʵ�飮 
��1���á��ɳ鶯����˿�����桰ֱ��Ͷ����Ƭ�����ŵ��� ��
��2��˵��SO2���������ʵ����������װ��C�������� ��
��3����Ӧһ��ʱ������Ƕ��Թ�A����Һ�Ľ������ӽ���̽���������������⣺
��������裺����1��ֻ����Fe3+��
����2��ֻ����Fe2+��
����3������Fe2+ �� ����Fe3+ ��
�������ʵ�鷽����֤����3��
��ѡ�Լ���ϡ���ᡢKMnO4��Һ��KSCN��Һ��NaOH��Һ��H2O2��Һ��
ʵ�鲽�� | Ԥ������ |
����һ���ý�ͷ�ι�ȡ��A�Թ��е���Һ����ˮϡ�ͺ���װ���Թܢ��б��� | |
�����������Fe3+ �� ���Թܢ��У� | |
������������Fe2+ �� ���Թܢ��У� |
��4����֪C+2H2SO4��Ũ�� ![]() 2SO2��+CO2��+2H2O���÷�Ӧ����Ũ������ԣ�
2SO2��+CO2��+2H2O���÷�Ӧ����Ũ������ԣ�
A����ˮ�� B��ǿ������ C����ˮ��
��Ҫ��֤��Ӧ������ͬʱ����SO2�����CO2���壬��ѡ�������Լ�����ʵ�飺
��NaOH��Һ��Ʒ����Һ����ˮ��Ca��OH��2��Һ��ѡ������Լ������ź�����˳��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʾ�������ˮ���������������ǵ��ǣ�
A. ��ѿ�� B. ���� C. ���� D. ��ά��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͬѧΪ�Ƶô�����Fe��OH��2 �� ʹ����ͼ��ʾ��װ�ã�A������Fe��H2SO4 �� B������NaOH��Һ�� 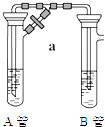
��1��ͬѧ�ף��ȼн�ֹˮ��a��ʹA�ܿ�ʼ��Ӧ����B���й۲쵽�������� ��
��2��ͬѧ�ң��ȴ�a��ʹA���з�Ӧһ��ʱ����ټн�ֹˮ��a�� ʵ������B���й۲쵽�������� ��
B�з�����Ӧ�����ӷ���ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E����������������ɵĿ����Ի����������������ʵ������У����Ӳ����ظ���ϣ���
������ | Na+��Mg2+��Al3+��Ba2+��Fe3+ |
������ | OH����Cl����CO |
�ֱ�ȡ���ǽ���ʵ�飬������£�
��A��Һ��D��Һ��ϣ�û����������
�ڵ�B��Һ���뵽D��Һ��ʱ���г�����������������B��Һ������ȫ����ʧ��
�۽�E��Һ���ȣ��г������ɣ�
�ݴ��ƶϣ�A ��B ��C ��D ��E ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��MԪ�ص�һ��ԭ��ʧȥ2�����ӣ���2������ת�Ƶ�YԪ�ص�����ԭ�����γ����ӻ�����Z������˵����ȷ���ǣ� ��
A. Z���۵�ϵ� B. Z���Ա�ʾΪM2Y
C. M���Ӻ�Y���ӵĺ�������Ų���ͬ D. M�γ�+2��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й��Ը߷���Ҳ���������Ը߷���������һ���ڲʵ�ӫ���������ģ���ɵ�·������Ӧ�ýϹ�����߷��Ӳ��ϣ���ṹ��ʽ����

�Իش��������⣺
��1����һ�������£��ø߾���ɷ����ķ�Ӧ��(��д���)________��
���ӳɷ�Ӧ����������Ӧ������ȥ��Ӧ����������Ӧ ��±����Ӧ
��2���ø߾����ڴ�����������ˮ��õ���Է���������С�IJ���A��A��ͬ���칹���ж��֣����к��б����� ���ұ��������������ڶ�λ��ȡ���������ʵĽṹ��ʽ������__________________��
���ұ��������������ڶ�λ��ȡ���������ʵĽṹ��ʽ������__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������м������Ӽ����й��ۼ����ǣ� ��
A. KOH B. H2O C. CaCl2 D. Cl2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں����ܱ������п�����Ϊ2NO2(g) ![]() 2NO(g)+O2(g)�ﵽƽ��״̬�ı�־��( )
2NO(g)+O2(g)�ﵽƽ��״̬�ı�־��( )
�ٵ�λʱ��������n mol O2��ͬʱ����2n mol NO2���ڵ�λʱ��������n mol O2��ͬʱ����2n mol NO���ۻ���������ɫ���ٸı䣻�ܻ��������ܶȲ��ٸı��״̬���ݻ�������ƽ����Է����������ٸı��״̬�����������NO��O2�����ʵ���֮�ȱ��ֺ㶨�����������NO��NO2�����ʵ���֮�ȱ��ֺ㶨
A. �٢ۢݢ� B. �ڢܢ� C. �٢ۢ� D. �٢ڢۢܢ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com