
(8分)某温度下的水溶液中,c(H+)=10-xmol/L,c(OH-)=10-y mol/L。x与y的关系如图所示:
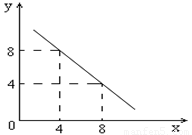
(1)该温度下水的离子积为 (填具体数值);该温度 常温(填“高于”、“低于”或“等于”)。
(2)该温度下0.01 mol/L NaOH溶液的pH为 。
(3)除了用pH外,科学家还建议用酸度(AG)来表示溶液的酸碱性: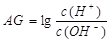 。则该温度下,0.01mol/L盐酸的酸度AG= 。
。则该温度下,0.01mol/L盐酸的酸度AG= 。
科目:高中化学 来源: 题型:
 在某温度下的水溶液中,c(H+)=10x mol?L-1,c(OH-)=10ymol?L-1,x与y关系如图所示.
在某温度下的水溶液中,c(H+)=10x mol?L-1,c(OH-)=10ymol?L-1,x与y关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)0.1mol/LNa2CO3溶液呈
(1)0.1mol/LNa2CO3溶液呈查看答案和解析>>
科目:高中化学 来源: 题型:
 在某温度下的水溶液中,c(H+)=10x mol/L,c(OH-)=10y mol/L,x与y的关系如图所示:
在某温度下的水溶液中,c(H+)=10x mol/L,c(OH-)=10y mol/L,x与y的关系如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
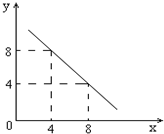 某温度下的水溶液中,c(H+)=10-xmol/L,c(OH-)=10-y mol/L.x与y的关系如图所示:
某温度下的水溶液中,c(H+)=10-xmol/L,c(OH-)=10-y mol/L.x与y的关系如图所示:| c(H+) | c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com