
| A. | 1 | B. | $\frac{1{0}^{-14-a-b}}{a}$ | C. | $\frac{1{0}^{a+b-14}}{a}$ | D. | $\frac{1{0}^{a-b}}{a}$ |
分析 室温下,HCl是强电解质,所以pH=a的盐酸中c(HCl)=10-a mol/L,一水合氨是弱电解质,所以pH=b且电离度为a的氨水中c(NH3.H2O)=$\frac{1{0}^{b-14}}{α}$mol/L,xL pH=a的盐酸溶液和yL pH=b的电离度为α的氨水恰好完全中和,说明二者的物质的量相等,据此分析解答.
解答 解:室温下,HCl是强电解质,所以pH=a的盐酸中c(HCl)=10-a mol/L,一水合氨是弱电解质,所以pH=b且电离度为a的氨水中c(NH3.H2O)=$\frac{1{0}^{b-14}}{α}$mol/L,xL pH=a的盐酸溶液和yL pH=b的电离度为α的氨水恰好完全中和,说明二者的物质的量相等,则10-axmol=$\frac{1{0}^{b-14}}{α}$ymol,则$\frac{x}{y}$=$\frac{1{0}^{a+b-14}}{a}$,故选C.
点评 本题考查酸碱混合溶液定性判断,为高频考点,正确计算氨水浓度是解本题关键,利用二者关系式分析解答,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 高炉炼铁的过程是通过置换反应得到铁 | |
| B. | 用直接加热氧化铝的方法冶炼得到铝 | |
| C. | 高温加热氧化镁和碳的混合物可以制单质镁 | |
| D. | 硫化亚铜与氧气反应炼铜的过程不属于氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2CH2CH3的三个碳原子在一条直线 | |
| B. | CH2=CHCH3三个碳原子共平面 | |
| C. | 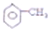 所有原子共平面 所有原子共平面 | |
| D. | CH4所有原子共平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ②③ | C. | ⑤⑥ | D. | ②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 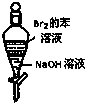 如图实验:振荡后静置,上层溶液颜色保持不变 如图实验:振荡后静置,上层溶液颜色保持不变 | |
| B. | 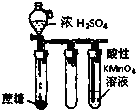 如图实验:酸性KMnO4溶液中出现气泡,且颜色逐渐褪去 如图实验:酸性KMnO4溶液中出现气泡,且颜色逐渐褪去 | |
| C. | 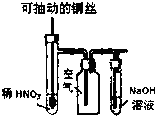 如图实验Ⅲ:微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终保持无色 如图实验Ⅲ:微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终保持无色 | |
| D. | 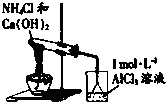 如图实验IV:烧杯中先出现白色沉淀,后溶解 如图实验IV:烧杯中先出现白色沉淀,后溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
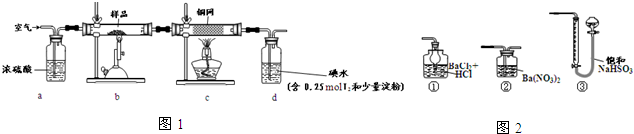
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X、Y可能在同一周期 | B. | X在Y的前一周期 | ||
| C. | X一定是金属元素 | D. | X一定是第三周期ⅡA或ⅣA族元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2使溴水褪色,显示了SO2的漂白性 | |
| B. | SO2使溴水褪色,显示了SO2的还原性 | |
| C. | 从溴水中提取单质溴,可以用乙醇进行萃取 | |
| D. | SO2使溴水褪色和使品红褪色原理相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com