

【题目】某无色溶液中含有大量的Ba2+、NH ![]() 、Cl﹣ , 在该溶液中还可能大量存在的离子是( )
、Cl﹣ , 在该溶液中还可能大量存在的离子是( )
A.Fe3+
B.CO ![]()
C.OH﹣
D.Mg2+
【答案】D
【解析】解:溶液无色时可排除 Cu2+、Fe2+、Fe3+、MnO![]() 等有色离子的存在,
等有色离子的存在,
A.Fe3+为有色离子,不满足溶液无色的要求,故A错误;
B.CO ![]() 与Ba2+发生反应,在溶液中不能大量共存,故B错误;
与Ba2+发生反应,在溶液中不能大量共存,故B错误;
C.OH﹣、NH![]() 反应,在溶液中不能大量共存,故C错误;
反应,在溶液中不能大量共存,故C错误;
D.Mg2+为无色离子,Mg2+不与Ba2+、NH![]() 、Cl﹣反应,在溶液中能够大量共存,故D正确;
、Cl﹣反应,在溶液中能够大量共存,故D正确;
故选D.
无色溶液可排除 Cu2+、Fe2+、Fe3+、MnO![]() 等有色离子的存在,
等有色离子的存在,
A.铁离子为有色离子,不满足溶液无色的条件;
B.碳酸根离子与钡离子反应生成碳酸钡沉淀;
C.铵根离子与氢氧根离子反应;
D.镁离子为无色离子,不与钡离子、铵根离子和氯离子反应.


科目:高中化学 来源: 题型:
【题目】某学习小组在实验室制取CO2气体的过程中,不慎用到了浓盐酸,导致制得的CO2气体中混有HCl气体,他们设计了如下除去HCl气体并探究CO2与过氧化钠(Na2O2)反应的实验。请回答下列问题:
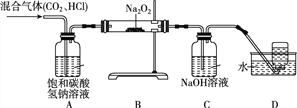
(1)装置A的作用是___________________________。
(2)为确定反应后装置B硬质玻璃管中固体的成分,小组同学取适量固体于试管中,加入足量的蒸馏水溶解形成溶液M,无气泡产生,则该固体中不含________,该小组同学继续进行探究。
【提出问题】反应后硬质玻璃管中固体的成分是什么?
(3)【做出猜想】猜想一:Na2CO3;猜想二:NaOH;猜想三:Na2CO3和NaOH
经过讨论,大家一致认为猜想二不合理,理由是_____________________________(用化学反应方程式表示)。
(4)【实验验证】小组同学取上述形成的溶液M于试管中,向其中加入过量的____________________溶液,若产生白色沉淀,过滤,向滤液中滴加几滴酚酞试液,溶液变红,则证明猜想三成立。
(5)【交流反思】小组中有同学认为,将上述滤液中滴加的酚酞试液换成硝酸铜溶液,也能得出同样的结论,你认为该同学的观点_____________(填“正确”或“错误”),理由是:____________________________________________(用化学反应方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】每年6月5日为世界环境日.下列有关环保建议不能采纳的是( )
A.开发利用太阳能
B.提倡垃圾分类处理
C.改进汽车尾气净化技术
D.将工业废水直接排放
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各溶液中,Na+ 物质的量浓度最大的是( )
A. 4 L 0.5 mol/L NaCl溶液 B. 5 L 0.4 mol/L NaOH溶液
C. 2 L 0.15 mol/L Na3PO4溶液 D. 1 L 0.3 mol/L Na2SO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时在2L密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的浓度变化如图1所示;若保持其他条件不变,温度分别为T1和T2(T2>T1)时,Y的体积分数(或Y的物质的量分数)与时间的关系如图2所示。则下列结论正确的是( )
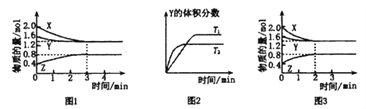
A. 容器中发生的反应可表示为:4X(g)+Y(g)![]() 2Z(g)
2Z(g)
B. 反应进行的前3min内,用X表示的反应速率v(X)=0.3mol/(L·min)
C. 升高温度,反应的化学平衡常数K增大
D. 若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家积极探索新技术对CO2进行综合利用。
Ⅰ.CO2可用来合成低碳烯烃:2CO2(g)+6H2(g)![]() CH2=CH2(g)+4H2O(g) △H=akJ/mol
CH2=CH2(g)+4H2O(g) △H=akJ/mol
请回答:
(1)已知:H2和CH2=CH的燃烧热分别是285.8kJ/mol和1411.0kJ/mol,且H2O(g)![]() H2O((1)△H=-44.0kJ/mol,则a=________kJ/mol。
H2O((1)△H=-44.0kJ/mol,则a=________kJ/mol。
(2)上述由CO2合成CH2=CH2的反应在________下自发进行(填“高温”或“低温”)。
(3)在体积为1L的恒容密闭容器中,充入3molH2和1molCO2,测得温度对CO2的平衡转化率和催化剂催化效率的影响如图1所示。下列说法正确的是________。
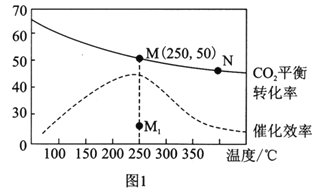
A.平衡常数大小:KMN
B.其他条件不变,若不使用催化剂,则250℃时CO2的平衡转化率可能位于点M1
C.图1中M点时,乙烯的体积分数为7.7%
D.当压强或n(H2)/n(CO2)不变时均可证明化学反应已达到平衡状态
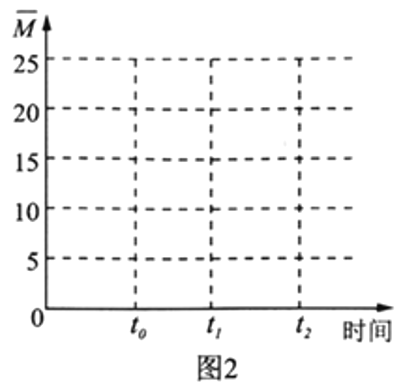
(4)保持温度不变,在体积为V L的恒容容器中以n(H2)∶n(CO2)=3∶1的投料比加入反应物,t0时达到化学平衡。请在图2中作出容器内混合气体的平均相对分子质量![]() 随时间变化的图象。___________
随时间变化的图象。___________
Ⅱ.利用“Na-CO2”电池将CO2变废为宝。我国科研人员研制出的可充电“Na-CO2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为4Na+3CO2![]() 2Na2CO3+C。放电时该电池“吸入”CO2,其工作原理如图3所示:
2Na2CO3+C。放电时该电池“吸入”CO2,其工作原理如图3所示:
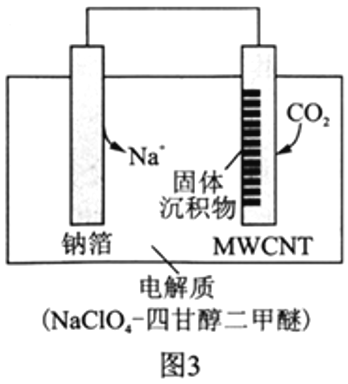
(5)放电时,正极的电极反应式为__________________。
(6)若生成的Na2CO3和C全部沉积在正极表面,当转移0.2mole-时,正极增加的质量为_______g。
(7)选用高氯酸钠四甘醇二甲醚做电解液的优点是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一个体重50kg的健康人,体内约含有2g铁,这2g铁在人体内不是以单质的形式存在,而是以Fe2+和Fe3+的形式存在.正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁.服用维生素C,可使食物中Fe3+还原成Fe2+ , 有利于人体吸收.
(1)在人体中进行Fe2+ ![]() Fe3+的转化时,①中的Fe2+作剂,②中的Fe3+作剂.
Fe3+的转化时,①中的Fe2+作剂,②中的Fe3+作剂.
(2)“服用维生素C,可使食物中的Fe3+还原成Fe2+”这句话指出,维生素C在这一反应中作剂.
(3)市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸(HCl)的作用下转化成亚铁盐,此反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于化学科学的说法,正确的是:
A.化学是在质子变化的层次上研究物质的一门基础学科
B.化学学科的特征是从宏观和微观两个角度认识物质
C.化学学科研究物质性质但不能创造出新物质
D.化学学科表征物质的方法与物理学科完全相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com