
已知25℃时有关弱酸的电离平衡常数:
|


科目:高中化学 来源: 题型:
已知25℃时有关弱酸的电离平衡常数:
|
查看答案和解析>>
科目:高中化学 来源: 题型:
已知25℃时有关弱酸的电离平衡常数:
|
查看答案和解析>>
科目:高中化学 来源: 题型:
已知25℃时有关弱酸的电离平衡常数:
|
查看答案和解析>>
科目:高中化学 来源: 题型:
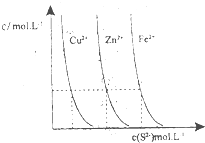 以下是对化学反应变化过程及结果的研究.按要求回答问题:
以下是对化学反应变化过程及结果的研究.按要求回答问题:| 弱酸化学式 | CH3COOH | HCN | H2CO |
| 电离平衡常数(25℃) | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K1=5.6×10-11 |
| 放电 |
| 通电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知25℃时有关弱酸的电离平衡常数.下列选项错误的是
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com