
在其他条件不变时,改变某一条件对A2(g)+3B2(g)  2AB3(g)化学平衡状态的影响,得到如右图所示的变化规律(T表示温度)。下列结论正确的是
2AB3(g)化学平衡状态的影响,得到如右图所示的变化规律(T表示温度)。下列结论正确的是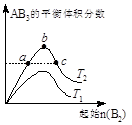
A.a、c两点A2的转化率相等
B.向a点的平衡体系中加入A2,可达到b点的平衡状态
C.b点时,平衡体系中A、B原子数之比最接近于1:3
D.正反应一定是吸热反应,且T2>T1
科目:高中化学 来源: 题型:单选题
25℃和1.01×105Pa时,反应:2N2O5(g) = 4NO2(g)+O2(g) △H= +56.76kJ/mol,自发进行的原因是
| A.是吸热反应 | B.是放热反应 |
| C.是熵减少的反应 | D.熵增大效应大于能量效应。 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
如图②为恒压容器,①③④为恒容容器,起始加入物如下,且起始容积均相等,维持恒温的条件下发生反应:2SO2(g)+O2(g)  2SO3(g) △H = –197kJ/mol达平衡后,各容器内放出热量Q1、Q2、Q3和Q4的大小关系正确的是
2SO3(g) △H = –197kJ/mol达平衡后,各容器内放出热量Q1、Q2、Q3和Q4的大小关系正确的是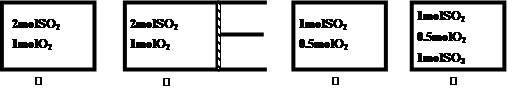
| A.197>Q1>Q2 | B.Q1>2Q3 | C.Q1=Q4 | D.Q3<Q4 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在25℃和1.01×105Pa时,2N2O5(g)=4NO2(g) + O2(g);△H=+56.7kJ/mol,能自发进行的合理解释是( )
| A.是吸热反应 | B.是放热反应 | C.是熵减反应 | D.是熵增效应大于能量效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
2012年是勒夏特列诞生192周年,下列叙述中,不用平衡移动原理解释的是 ( )
| A.红棕色的NO2,加压后颜色先变深后变浅 |
| B.高压比常压有利于合成SO3的反应 |
| C.由H2(g)、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深 |
| D.黄绿色的氯水光照后颜色变浅 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
对于化学反应3W(g)+2X(g)=4Y(g)+3Z(g),下列反应速率关系中,正确的是
A.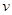 (W)=3 (W)=3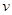 (Z) (Z) | B.2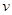 (X)=3 (X)=3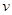 (Z) (Z) |
C.2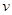 (X)= (X)=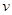 (Y) (Y) | D.3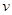 (W)=2 (W)=2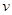 (X) (X) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
向甲、乙两个容积均为1L的恒容密闭容器中,分别充入2mol A、2 mol B和1 mol A、1 mol B。相同条件下,发生下列反应:A(g)+B(g) xC(g)
xC(g) 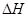 <0。测得两容器中c(A)随时间t的变化如图所示:
<0。测得两容器中c(A)随时间t的变化如图所示: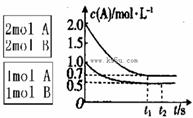
下列说法中正确的是
A.x可能等于2也可能等于1
B.向平衡后乙容器中充入氦气可使c(A)增大
C.将乙容器单独降温可使乙容器内各物质的体积分数与甲容器内的相同
D.若向甲容器中再充入2mol A、2 mol B,则平衡时甲容器中0.7 mol<n(B)<1.4 mol
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
将0.5mol PCl5充入体积为1L的密闭容器中,发生反应PCl5 PCl3+Cl2,一段时间后测得PCl5的浓度为0.3mol/L,且这段时间内的平均反应速率v(PCl5)="0.4" mol/(L·min),则这段时间为
PCl3+Cl2,一段时间后测得PCl5的浓度为0.3mol/L,且这段时间内的平均反应速率v(PCl5)="0.4" mol/(L·min),则这段时间为
| A.80s | B.45s | C.30s | D.15s |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com