
已知X的基态原子L层电子数是K层电子数的2倍,Y的基态原子最外层电子排布式为nsnnpn+2,则X的电负性比Y的________(填“大”或“小”)。
科目:高中化学 来源: 题型:
Nomex纤维是一种新型阻燃纤维,其结构简式为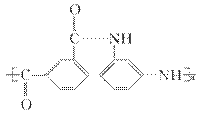 ,据此可以推知在一定条件下,以等物质的量发生缩聚反应生成该物质的两种单体是( )。
,据此可以推知在一定条件下,以等物质的量发生缩聚反应生成该物质的两种单体是( )。
A.间苯二甲酸和邻苯二胺
B.间苯二甲酸和间苯二胺
C.间苯二甲酸和对苯二胺
D.对苯二甲酸和对苯二胺
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E、F代表6种元素。请填空:
(1)A元素基态原子的最外层有2个未成对电子,次外层有2个电子,其元素符号为__________。
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B的元素符号为________,C的元素符号为________。
(3)D元素的正三价离子的3d轨道为半充满,D的元素符号为________,其基态原子的电子排布式为_________________________________________________________________。
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,E的元素符号为________,其基态原子的电子排布式为__________________________________。
(5)F元素的原子最外层电子排布式为nsnnpn+1,则n=________;原子中能量最高的是________电子。
查看答案和解析>>
科目:高中化学 来源: 题型:
前四周期原子序数依次增大的元素A、B、C、D中,A和B的价电子层中未成对电子均只有1个,并且A-和B+的电子数相差为8;与B位于同一周期的C和D,它们价电子层中的未成对电子数分别为4和2,且原子序数相差为2。
四种元素中的第一电离能最小的是__________,电负性最大的是__________。(填元素符号)
查看答案和解析>>
科目:高中化学 来源: 题型:
关于1s、2s、3s、4s原子轨道的说法,正确的是 ( )
A.电子只能在电子云轮廓图中运动
B.轨道不同,电子云轮廓图形状相同
C.轨道数目相同,电子云轮廓图形状、大小完全相同
D.能层不同,电子云轮廓图形状也不相同
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X、Y是主族元素,I为电离能,单位是kJ·mol-1。请根据下表数据判断,错误的是 ( )
| 元素 | I1 | I2 | I3 | I4 |
| X | 500 | 4 600 | 6 900 | 9 500 |
| Y | 580 | 1 800 | 2 700 | 11 600 |
A.元素X的常见化合价是+1价
B.元素Y是ⅢA族元素
C.元素X与氯形成化合物时,化学式可能是XCl
D.若元素Y处于第3周期,它可与冷水剧烈反应
查看答案和解析>>
科目:高中化学 来源: 题型:
实验测得:101 kPa时,1 mol H2完全燃烧生成液态水,放出285.8 kJ的热量;1 mol CH4完全燃烧生成液态水和CO2,放出890.3 kJ的热量。下列热化学方程式的书写正确的是( )
①CH4(g)+2O2(g)===CO2(g)+2H2O(l)
ΔH=890.3 kJ·mol-1
②CH4(g)+2O2(g)===CO2(g)+2H2O(l)
ΔH=-890.3 kJ·mol-1
③CH4(g)+2O2(g)===CO2(g)+2H2O(g)
ΔH=-890.3 kJ·mol-1
④2H2(g)+O2(g)===2H2O(l)
ΔH=-571.6 kJ·mol-1
A.仅有② B.仅有②④ C.仅有②③④ D.全部符合要求
查看答案和解析>>
科目:高中化学 来源: 题型:
如何用所提供的试剂和方法除去各粉末状混合物中的杂质(括号内为杂质)。将所选答案的编号填入下表内相应的空格内(如果不需要外加试剂,则对应答案栏可空着)。
可供选择的试剂:A.盐酸 B.氢氧化钠溶液 C.氧气
D.水 E.二氧化碳
可选用的操作:①水洗 ②加热 ③高温灼烧 ④过滤
⑤结晶
| 粉末状混合物 | 选择的试剂 | 选用的操作 | |
| (1) | CaCO3(SiO2) | ||
| (2) | NaCl(SiO2) | ||
| (3) | SiO2(Fe2O3) | ||
| (4) | SiO2(CaCO3) | ||
| (5) | SiO2(NH4Cl) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com