
| A. | 盐类的水解过程是中和反应的逆过程,是吸热过程 | |
| B. | 易水解的盐溶于水后,都抑制了水的电离 | |
| C. | 易水解的盐溶液中,水电离出的以游离态存在的H+和OH-的浓度永远相等 | |
| D. | 易水解的盐溶液肯定不是中性的 |
分析 A.根据盐的水解原理可知,盐的水解是中和反应的逆过程,中和反应是放热反应,则盐的水解为吸热反应;
B.易水解的盐溶于水能够促进水的电离;
C.水解过程中,水电离的氢离子或氢氧根离子需要结合弱酸根或弱碱根离子;
D.易水解的盐溶液可能为中性的,如醋酸铵溶液.
解答 解:A.盐的水解是盐和水反应生成对应的酸和碱的过程,盐类水解生成是中和反应的逆过程,中和反应放热,则盐的水解是吸热的,故A正确;
B.弱酸根或弱碱根离子水解后结合水电离的氢离子或氢氧根离子,促进了水的电离,故B错误;
C.在盐的水解过程中,水电离出的氢离子、氢氧根离子会结合弱酸根离子或弱碱根离子,所以溶液中水电离的以游离态存在的氢离子、氢氧根离子的浓度不一定相等,故C错误;
D.对于弱酸弱碱盐,弱酸根离子的水解程度与弱碱根离子的水解程度相同,如醋酸铵溶液,则其溶液可以为中性,故D错误;
故选A.
点评 本题考查了盐的水解原理及其影响因素,题目难度中等,注意掌握盐的水解原理及影响因素,明确盐的水解过程促进了水的电离,且能够水解的盐溶液不一定为酸性或碱性,有可能为中性,如醋酸铵溶液.


科目:高中化学 来源: 题型:解答题
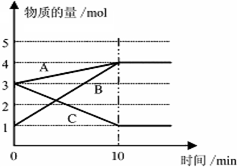 将一定量的A、B、C三种物质(都是气体)放入固定体积为10L的密闭容器中,一定条件下发生反应,一段时间内测得各物质的物质的量变化如图所示.
将一定量的A、B、C三种物质(都是气体)放入固定体积为10L的密闭容器中,一定条件下发生反应,一段时间内测得各物质的物质的量变化如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化合物 | 燃烧热 | 化合物 | 燃烧热 |
| 甲烷 | 891.0 | 正丁烷 | 2878.0 |
| 乙烷 | 1560.8 | 异丁烷 | 2869.6 |
| 丙烷 | 2221.5 | 2-甲基丁烷 | 3531.3 |
| A. | 热稳定性:正丁烷<异丁烷 | |
| B. | 乙烷燃烧的热化学方程式为: 2C2H6(g)+7O2(g)→4CO2(g)+6H2O(g)△H=-1560.8KJ/mol | |
| C. | 正戊烷的燃烧热不超过3530 KJ/mol | |
| D. | 相同质量的烷烃,碳的质量分数越大,完全燃烧放出的热量越多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该温度下纯重水的pD=7 | |
| B. | 在1L D2O的溶液中溶解0.01mol NaOD(设溶液体积为1L),其中pD=12 | |
| C. | 向100mL 0.25mol•L-1的DCl重水溶液中加入50mL 0.2mol•L-1的NaOD的重水溶液,其中pD=2 | |
| D. | 在1L D2O中溶解0.01mol DCl(设溶液的体积为1L),其中pD=2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
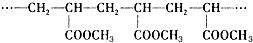
| A. | 它是缩聚反应的产物 | B. | 高分子的分子式是C4H6O2 | ||
| C. | 合成它的单体是CH2=CHCOOCH3 | D. | 高分子的相对分子质量是86 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| Z | W | ||
| X | Y |
| A. | X元素最高价氧化物化学式为X2O3 | |
| B. | 原子半径:X>Y>Z>W | |
| C. | 最简单气态氢化物的热稳定性:W>Y | |
| D. | Y元素的最高价氧化物既能与NaOH溶液反应,也能与HF溶液反应,属于两性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
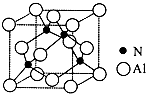 Ⅰ. 已知氮化铝的晶胞结构如图所示,请回答下列问题.
Ⅰ. 已知氮化铝的晶胞结构如图所示,请回答下列问题.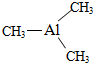 ,则其
,则其查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子半径:S2->O2->Na+>Al3+ | B. | 热稳定性:HCl>H2S>PH3>AsH3 | ||
| C. | 电负性:F>O>N>C | D. | 第一电离能:F>O>N>C |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com