
A、200mL 1mol/L Al2(SO4)3溶液中,SO
| ||
| B、标准状况下,22.4L Cl2和HCl的混合气体中含分子总数为2×6.02×1023 | ||
C、0.1mol SO
| ||
| D、78g Na2O2与水完全反应后转移电子总数为:2×6.02×1023 |


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、配制一定物质的量浓度稀硫酸时,量取一定体积的浓硫酸注入烧杯,加水稀释冷却后转移到容量瓶中 |
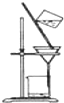
| B、洗涤沉淀时(见图),向漏斗中加适量水,搅拌并滤干 |
| C、用干燥的pH试纸可测得新制氯水的pH=2 |
| D、配制FeSO4溶液时,常常向溶液中加入少量铁粉,并且现配现用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ca2+、Al3+、CO32ˉ、AlO2- |
| B、Cu2+、Cl-、Na+、NO3- |
| C、Fe2+、H+、SO42ˉ、NO3ˉ |
| D、Mg2+、NO3-、K+、Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:1 | B、1:2 |
| C、1:3 | D、1:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| H | + 4 |
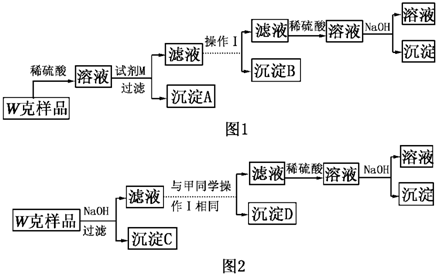
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、第15列元素的最高价氧化物为R2O5 |
| B、第2列元素中肯定没有非金属元素 |
| C、L层电子数为偶数的所有主族元素所在族的族序数与元素原子L层电子数相等 |
| D、M层电子数为奇数的所有主族元素所在族的族序数与元素原子M层电子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用亚硫酸钾溶液吸收硫酸工业尾气中的SO2:SO2+SO32-+H20=2HSO3- |
| B、向AlCl3溶液中加入过量的NaOH溶液:Al3++3OH-=Al(OH)3↓ |
| C、高锰酸钾与足量浓盐酸反应制氯气:2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O |
| D、漂白粉溶液中,通入过量的二氧化碳:Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com