
分析 在调至中性的亚硫酸钠溶液中加入甲醛水溶液,经充分反应后,产生的氢氧化钠的物质的量与甲醛的物质的量相等;
(1)将4.00mL甲醛水溶液加入到经调至中性的亚硫酸钠溶液中,充分反应后,得到溶液中含有NaOH,由硫酸的物质的量可得NaOH,以此确定甲醛的物质的量,进而计算浓度;若滴定管规格为50mL,如硫酸全部反应,体积为50mL,则可知消耗硫酸的物质的量,可知需要甲醛的物质的量,结合其浓度,可确定体积;
(2)根据HCHO分子中碳原子化合价为0价,HCHO+2Cu(OH)2$\stackrel{△}{→}$HCOOH+Cu2O↓+2H2O,HCOOH中碳原子化合价为+2价,化合价升高,还原剂,具有还原性,1个HCHO转移2个电子;根据价层电子对互斥模型判断.
解答 解:(1)产生的氢氧化钠的物质的量与甲醛的物质的量相等,n(H2SO4)=1.100mol•L-1×0.02L=0.022mol,将4.00mL甲醛水溶液加入到经调至中性的亚硫酸钠溶液中,充分反应后,得到溶液中含有NaOH,加入硫酸发生反应:H2SO4+2NaOH=Na2SO4+2H2O,则n(HCHO)=n(NaOH)=2n(H2SO4)=0.022mol×2=0.044mol,c(HCHO)=$\frac{0.044mol}{0.004L}$=11mol/L;
若滴定管规格为50mL,如硫酸全部反应,体积为50mL,则可知消耗硫酸的物质的量为0.05L×11mol/L=0.055mol,则n(HCHO)=n(NaOH)=2n(H2SO4)=0.11mol,甲醛水溶液取样不能超过的体积为V=$\frac{n}{c}$=$\frac{0.11mol}{11mol/L}$=0.01L=10mL;
故答案为:11;10;
(2)HCHO分子中碳原子化合价为0价,HCHO+2Cu(OH)2$\stackrel{△}{→}$HCOOH+Cu2O↓+2H2O,HCOOH中碳原子化合价为+2价,化合价升高,还原剂,具有还原性;每1mol甲醛参加反应转移的电子数为2NA,即1.204×1024,甲醛分子内碳原子形成3个σ键,无孤对电子,杂化方式为sp2杂化,立体构型为平面三角形;
故答案为:还原性;1.204×1024;sp2.
点评 本题以甲醛为载体综合考查物质的含量测定、杂化理论的应用,侧重于学生的分析,有利于培养学生良好的科学素养,提高学习的积极性,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 100 mL | B. | 45 mL | C. | 10 mL | D. | 15 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
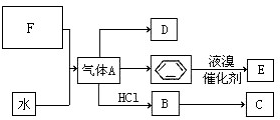 已知:C是一种合成树脂,用于制备塑料和合成纤维,D是一种植物生长调节剂,用它可以催熟果实.根据以下化学反应框图填空:
已知:C是一种合成树脂,用于制备塑料和合成纤维,D是一种植物生长调节剂,用它可以催熟果实.根据以下化学反应框图填空: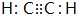 ;C的结构简式
;C的结构简式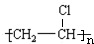 ;
; +Br2 $\stackrel{FeBr_{3}}{→}$
+Br2 $\stackrel{FeBr_{3}}{→}$ +HBr,其反应类型为取代反应;
+HBr,其反应类型为取代反应;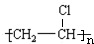 ,其反应类型为加聚反应.
,其反应类型为加聚反应.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验组别 | 10%硫酸体积/mL | 温度/℃ | 其他物质 |
| Ⅰ | 2.0mL | 20 | / |
| Ⅱ | 2.0mL | 20 | 少量MnSO4粉末 |
| Ⅲ | 2.0mL | 30 | / |
| Ⅳ | 1.0mL | 20 | 1.0mL蒸馏水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③⑥①②⑤④ | B. | ⑤①②⑥④③ | C. | ⑤④③②①⑥ | D. | ③①②④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 室温下用广范pH试纸测得某氯水的pH=4 | |
| B. | 酸式滴定管的润洗操作:关闭滴定管活塞,往上口加入3~5mL待装液,倾斜着转动滴定管,使液体润湿滴定管内壁,然后将液体从上口倒出,重复此操作2~3次 | |
| C. | 若酸碱中和滴定过程中用待测液润洗锥形瓶,则测定结果偏高 | |
| D. | 酸碱中和滴定的终点是指酸和碱恰好完全反应,此时溶液一定呈中性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硅(半导体材料) | B. | 二氧化硅(制光导纤维) | ||
| C. | Na2Si03 (用作粘合剂,俗称水玻璃) | D. | Al(OH)3(用作胃药,俗称人造刚玉) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

实验 记录 | ①Zn质量减少,Cu质量不变; ②外电路电流方向是:由Cu→Zn; ③SO42- 向Cu极移动; ④Zn电极发生氧化反应; ⑤正极反应式:Cu2++2e-═Cu |
| A. | ①②④ | B. | ②③④ | C. | ②④⑤ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 粗铜精炼时,与电源正极相连的是纯铜,阳极反应式为Cu-2e-═Cu2+ | |
| B. | 氢氧燃料电池的负极反应式:O2+2H2O+4e-═4OH- | |
| C. | 用惰性电极电解饱和食盐水时,阳极的电极反应式为2Cl--2e-═Cl2↑ | |
| D. | 钢铁发生电化学腐蚀的正极反应式:Fe-2e-═Fe2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com