

| 134×71.64% |
| 12 |
| 134×23.88% |
| 16 |
| 134-12×8-16×2 |
| 1 |
 ,A与B发生信息中反应,可知电石气与水反应生成B为CH3CHO,由C的分子式可知1分子A与2分子B反应,则C为
,A与B发生信息中反应,可知电石气与水反应生成B为CH3CHO,由C的分子式可知1分子A与2分子B反应,则C为 ,C发生氧化反应生成D、D酸化得到E,则D为
,C发生氧化反应生成D、D酸化得到E,则D为 ,E为
,E为 ,C与氢气发生加成反应生成芳香族化合物F,由F的分子式可知C中碳碳双键、醛基均发生加成反应,则F为
,C与氢气发生加成反应生成芳香族化合物F,由F的分子式可知C中碳碳双键、醛基均发生加成反应,则F为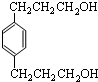 ,E与F发生水解反应生成链状高聚物G为
,E与F发生水解反应生成链状高聚物G为 ,据此解答.
,据此解答.| 134×71.64% |
| 12 |
| 134×23.88% |
| 16 |
| 134-12×8-16×2 |
| 1 |
 ,A与B发生信息中反应,可知电石气与水反应生成B为CH3CHO,由C的分子式可知1分子A与2分子B反应,则C为
,A与B发生信息中反应,可知电石气与水反应生成B为CH3CHO,由C的分子式可知1分子A与2分子B反应,则C为 ,C发生氧化反应生成D、D酸化得到E,则D为
,C发生氧化反应生成D、D酸化得到E,则D为 ,E为
,E为 ,C与氢气发生加成反应生成芳香族化合物F,由F的分子式可知C中碳碳双键、醛基均发生加成反应,则F为
,C与氢气发生加成反应生成芳香族化合物F,由F的分子式可知C中碳碳双键、醛基均发生加成反应,则F为 ,E与F发生水解反应生成链状高聚物G为
,E与F发生水解反应生成链状高聚物G为 ,
, ,反应③属于氧化反应、反应④属于加成反应,
,反应③属于氧化反应、反应④属于加成反应, ;氧化反应;加成反应;
;氧化反应;加成反应; +4Cu(OH)2+2NaOH
+4Cu(OH)2+2NaOH| △ |
 +2Cu2O↓+6H2O,
+2Cu2O↓+6H2O, +n
+n
| 浓硫酸 |
| △ |
 +(2n-1)H2O,
+(2n-1)H2O, +4Cu(OH)2+2NaOH
+4Cu(OH)2+2NaOH| △ |
 +2Cu2O↓+6H2O;
+2Cu2O↓+6H2O; +n
+n
| 浓硫酸 |
| △ |
 +(2n-1)H2O;
+(2n-1)H2O; )的同分异构体中能发生银镜反应且属芳香族化合物的有:
)的同分异构体中能发生银镜反应且属芳香族化合物的有: ,
, .
.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
 液反应生成盐;丙、戊可组成化合物M.
液反应生成盐;丙、戊可组成化合物M.查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
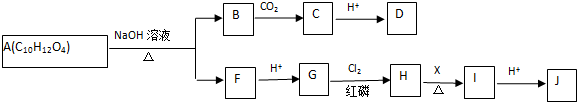
| Cl2 |
| 红磷 |
 +HCl
+HCl查看答案和解析>>
科目:高中化学 来源: 题型:
 二氧化氯(C1O2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.
二氧化氯(C1O2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③ | B、①③④ |
| C、①②④ | D、①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.l mol的2H35Cl分子中的中子数是2NA |
| B、标准状况下,一定量的铜与硝酸反应后生成22.4 LNO、NO2、N2O4的混合气体,则被还原的硝酸的分子数大于NA |
| C、100mL 1 mol Na[Al(OH)4]溶液中含有0.12NA个[Al(OH)4]- |
| D、1mol羟基和1mol氢氧根离子中的电子数和质子数均相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应过程中,电子转移数为2NA |
| B、固体生成物的质量为106g |
| C、CO可能有剩余 |
| D、反应后一定生成11.2升氧气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| KSP(25℃) | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
| A、向混合溶液中逐滴加入NaOH溶液,最先看到红褐色沉淀 |
| B、向溶液中加入双氧水,并用CuO粉末调节pH,过滤后可获较纯净的CuSO4溶液 |
| C、该溶液中c(SO42-):[c(Fe3+)+c(Fe2+)+c(Cu2+)=5:4 |
| D、将少量FeCl3粉末加入含Cu(OH)2的悬浊液中,其中c(Cu2+)增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com