
【题目】环之间共用一个碳原子的化合物称为螺环化合物。1,4-二氧杂螺[2.2]丙烷的结构简式为![]() 。下列说法正确的是
。下列说法正确的是
A. 1mol该有机物完全燃烧需要4molO2
B. 该有机物与 HCOOCH=CH2互为同分异构体
C. 该有机物的二氯代物有3种
D. 该有机物所有原子均处于同一平面
科目:高中化学 来源: 题型:
【题目】氮、磷及其化合物在工农业生产中都有重要用逾。
(1)基态磷原子价电子排布的轨道表示式为_____。
(2)元素B、N、O的第一电离能由大到小的顺序为_____。
(3)一种食品添加剂NaNO2中NO2﹣中心原子的杂化类型是_____,与NO2﹣互为等电子体的分子的化学式为_____(写1种)
(4)N2H4是火箭的燃料,与氧气的相对分子质量相同,它在常温常压下是液态,而氧气是气态,造成这种差异的主要原因是_____。
(5)磷化硼是一种耐磨涂料,它可用作金属的表面保护层,磷化硼可由三溴化硼和三溴化磷于高温下在氢气中反应合成。
①三溴化磷分子的空间构型是_____,三溴化硼键角是_____。
②磷化硼晶体晶胞如图所示,其中实心球为磷原子,在一个晶胞中磷原子空间堆积方式为_____,磷原子的配位数为是_____,该结构中有一个配位健,提供空轨道的原子是_____;已知该晶胞边长apm,阿伏加德罗常数为NA,则磷化硼晶体的密度为_____gcm﹣3。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中通入一定量的HI气体,使其在一定条件下发生反应:2HI(g)![]() H2(g)+I2(g)。下列叙述中,一定属于平衡状态的是
H2(g)+I2(g)。下列叙述中,一定属于平衡状态的是
A. HI、H2、I2的浓度相等
B. 混合气体的颜色不再变化
C. 混合气体的总压强不再变化
D. v(HI)∶v(H2)∶v(I2)=2∶1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等物质的量的A、B混合于2 L的密闭容器中,发生下列反应:3A(g)+B(g)=xC(g)+2D(g)。经5 min时测得D的浓度为1 mol·L-1,c(A):c(B)=3:5,C的平均反应速率是0.3 mol·L-1·min-1,求
(1)x值是多少? ___________
(2)5 min 时A的物质的量为多少?_____________
(3)B的平均反应速率为多少?___________
(4)B的转化率为多少?____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮族元素在化学领域具有重要的地位。请回答下列问题:
(1)基态氮原子的价电子轨道表示式为___________;第二周期的元素中,第一电离能介于B和N之间的元素有___________种。
(2)雌黄的分子式为As2S3,其分子结构如图所示:![]() As原子的杂化类型为___________。
As原子的杂化类型为___________。
(3)①向CuSO4溶液中加入少量氨水生成蓝色沉淀,继续加入氨水沉淀溶解,得到深蓝色透明溶液,向该溶液中加入一定量的乙醇,析出[Cu(NH3)4]SO4·H2O固体。SO42-的空间构型为___________;[Cu(NH3)4]SO4·H2O固体中含有的化学键有___________(填标号)。
A.离子键 B.共价键 C.氢键 D.金属键 E.配位键
若要确定[Cu(NH3)4]SO4·H2O是晶体还是非晶体,最科学的方法是进行___________实验。
②已知NF3与NH3分子的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,原因是___________。
(4)大π键可用![]() 表示,其中n、m分别代表参与形成大π键的原子个数和电子数,如苯分子中大π键表示为
表示,其中n、m分别代表参与形成大π键的原子个数和电子数,如苯分子中大π键表示为![]() 。N2O分子中的大π键表示为_________________。
。N2O分子中的大π键表示为_________________。
(5)立方氮化硼晶胞如图,其密度为ρg/cm3,氮化硼的摩尔质量为Mg/mol,阿伏加德罗常数的值为NA,硼原子的半径为r cm,则硼原子的空间占有率为____________________(用含有ρ、M、NA、r的代数式表示)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化二氯(C12O)是次氯酸的酸酐,用作氯化剂其部分性质如下:
物理性质 | 化学性质 |
常温下,C12O是棕黄色刺激性气体。 熔点:-120.6℃;沸点2.0℃ | C12O不稳定接触一般有机物易爆炸;它易溶于水,同时反应生成次氯酸。 |
实验室制备原理2Na2CO3+H2O+2Cl2![]() 2NaCl +2NaHCO3+ C12O, 现用下列装置设计实验制备少量C12O,并探究相关物质的性质。
2NaCl +2NaHCO3+ C12O, 现用下列装置设计实验制备少量C12O,并探究相关物质的性质。

(1)装置A中仪器X的名称为___________。
(2)若气体从左至右流动装置连接顺序是A、___________(每个装置限用一次)。
(3)装置F中盛装试剂的名称为___________。
(4)A中反应的离子方程式为___________。
(5)当D中收集适量液态物质时停止反应,设计简单实验证明B中残留固体中含有NaHCO3:___________。
(6)实验完成后取E中烧杯内溶液滴加品红溶液发现溶液褪色。该课题组设计实验探究溶液褪色的原因。
序号 | 0.1mol/LNaClO溶液/mL | 0.1mol/LNaCl溶液/mL | 0.1mol/LNaOH溶液/mL | H2O/mL | 品红溶液 | 现象 |
I | 5.0 | 0 | 0 | 5.0 | 3滴 | 较快褪色 |
II | 0 | 5.0 | a | 0 | 3滴 | 不褪色 |
III | 5.0 | 0 | 0 | 3滴 | 缓慢褪色 |
①a=___________。
②由上述实验得出的结论是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究表明,大气中氮氧化物和碳氢化合物受紫外线作用可产生二次污染物——光化学烟雾,其中某些反应过程如图所示。下列说法不正确的是

A. 整个过程中O3作催化剂
B. 反应III的方程式为O2+O===O3
C. 光化学烟雾中含甲醛、乙醛等刺激性物质
D. 反应I、反应Ⅱ均属于氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝是应用广泛的金属。以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质)为原料制备铝的一种工艺流程如下:

注:SiO2在“碱溶”时转化为铝硅酸钠沉淀。
(1)“碱溶”时生成偏铝酸钠的离子方程式为_____________________。
(2)向“过滤Ⅰ”所得滤液中加入NaHCO3溶液,溶液的pH_________ (填“增大”、“不变”或“减小”)。
(3)“电解Ⅰ”是电解熔融Al2O3,电解过程中作阳极的石墨易消耗,原因是___________。
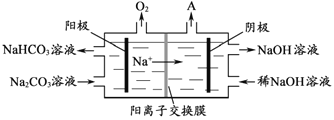
(4)“电解Ⅱ”是电解Na2CO3溶液,原理如图所示。阳极的电极反应式为_____________________,阴极产生的物质A的化学式为____________。
(5)铝粉在1000℃时可与N2反应制备AlN。在铝粉中添加少量NH4Cl固体并充分混合,有利于AlN的制备,其主要原因是_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com