
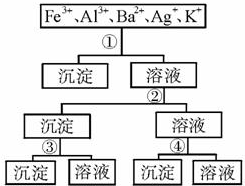
 用过量的H2SO4、NaOH、NH3、H2O、NaCl等溶液,按题如图所示步骤分开五种离子.则溶液①、②、③、④是( )
用过量的H2SO4、NaOH、NH3、H2O、NaCl等溶液,按题如图所示步骤分开五种离子.则溶液①、②、③、④是( )| A、①NaCl ②NaOH ③NH2?H2O ④H2SO4 |
| B、①H2SO4 ②NaOH ③NH3?H2O ④NaCl |
| C、①H2SO4 ②NH3?H2O ③NaOH ④NaCl |
| D、①NaCl ②NH3?H2O ③NaOH ④H2SO4 |


科目:高中化学 来源: 题型:
| A、采用绿色工艺,使原料尽可能转化为所需物质 |
| B、大量开采地下水,以满足社会需求 |
| C、开发利用绿色能源替代化石燃料 |
| D、严格执行机动车尾气排放标准 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①-d | B、②-a |
| C、③-c | D、④-b |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、引起空气发生化学变化 |
| B、产生杀菌消毒作用 |
| C、诱发动植物的基因突变 |
| D、造成病毒感染 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 物 质 | MgO | MgCl2 | Mg3N2 | Mg(NO3)2 | MgCO3 | Mg(OH)2 |
| 颜 色 | 白色 | 白色 | 淡黄色 | 白色 | 白色 | 白色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
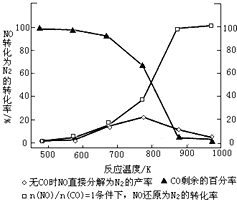 汽车使用乙醇汽油并不能减少NOx的排放,这使NOx的有效消除成为环保领域的重要课题.某研究小组在实验室以Ag-ZSM-5 为催化剂,测得NO转化为N2的转化率随温度变化情况如图.
汽车使用乙醇汽油并不能减少NOx的排放,这使NOx的有效消除成为环保领域的重要课题.某研究小组在实验室以Ag-ZSM-5 为催化剂,测得NO转化为N2的转化率随温度变化情况如图.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com