
| A. | NaOH、NaCl、HCl、Na2SO4 | B. | NaCl、Na2SO4、NaOH、HCl | ||
| C. | NaCl、NaOH、Na2SO4、HCl | D. | Na2SO4、NaOH、NaCl、HCl |
分析 分别将Ag+、Al3+、Mg2+、Ba2+离子以沉淀形式从溶液中分离出来,由于氢氧化钠能够与银离子、镁离子、铝离子反应,应该先用NaCl将Ag+转化成AgCl沉淀,然后用过量NaOH将Mg2+转化成Mg(OH)2沉淀,即NaCl应该放在NaOH之前;将偏铝酸根离子转化成Al(OH)3沉淀,需要加入酸,则HCl放在NaOH之后;而用Na2SO4除去Ba2+的操作不受限制,据此进行解答.
解答 解:分别将Ag+、Al3+、Mg2+、Ba2+离子以沉淀形式从溶液中分离出来,由于氢氧化钠能够与银离子、镁离子、铝离子反应,则应先用NaCl将Ag+转化成AgCl沉淀,然后用过量NaOH将Mg2+转化成Mg(OH)2沉淀,即NaCl应该放在NaOH之前,故AD错误;
将偏铝酸根离子转化成Al(OH)3沉淀,需要加入酸,则HCl放在NaOH之后,而用Na2SO4除去Ba2+的操作顺序不受限制,所以BC正确,
故选BC.
点评 本题考查物质的分离、提纯,题目难度中等,侧重于学生的分析能力和元素化合物知识的综合理解和运用的考查,为高频考点,把握物质的性质为解答该题的关键,注意满足“四种离子分别以沉淀形式从溶液中分离出来”.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
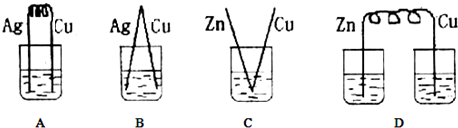
 用如图所示装置检验对应气体时,不能达到目的是( )
用如图所示装置检验对应气体时,不能达到目的是( ) | 生成的气体 | 试剂X | 试剂Y | |
| A | 电石与水反应制取的乙炔 | CuSO4 | Br2的CCl4溶液 |
| B | 证明苯与液溴的反应是取代反应而不是加成反应 | 水 | AgNO3溶液 |
| C | CH3CH2Br与NaOH乙醇溶液共热制取的乙烯 | 水 | KMnO4酸性溶液 |
| D | C2H5OH与浓硫酸加热至170℃制取乙烯 | NaOH溶液 | Br2的CCl4溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 燃着的酒精灯打翻起火,应用水扑灭 | |
| B. | 如果苯酚溶液沾到皮肤上,应立即用酒精洗涤 | |
| C. | 向2 mL2% AgNO3溶液中滴加浓氨水至沉淀刚好消失制备银氨溶液 | |
| D. | 向新制的Cu(OH)2悬浊液中滴入少量乙醛溶液,加热,观察到红色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl电离产生H+和Cl-,可判断HCl分子中存在离子键 | |
| B. | 阴、阳离子间通过静电引力所形成的化学键是离子键 | |
| C. | 化学变化过程,一定会破坏旧的化学键,同时形成新的化学键 | |
| D. | 不同元素组成的多原子分子中的化学键一定全是极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
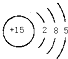 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:填空题
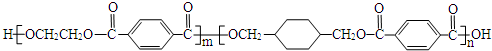
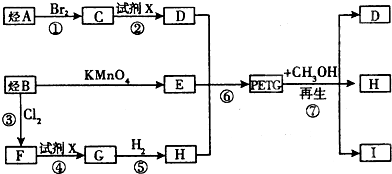
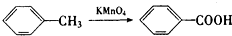

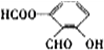 、
、 、
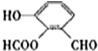
、
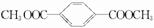 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢化物的沸点:Z一定高于Y | |
| B. | 最高价氧化物对应水化物的酸性:X强于Y | |
| C. | W、X、Y、Z都能分别与氯元素形成共价化合物 | |
| D. | 仅由W、Y、Z三种元素组成的化合物不可能属于盐类 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | CH4 | CO2 | CO | H2 |
| 体积分数 | 0.1 | 0.1 | 0.4 | 0.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com