

2- 4 |
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量吸收液于试管中,滴加3mol?L-1 H2SO4至溶液呈酸性,然后将所得溶液分置于A、B试管中. | |
| 步骤2:向A试管中滴加1~2滴 | 若溶液 否则,则假设2或3成立. |
| 步骤3:向B试管中滴加1~2滴 | 若溶液 否则,结合步骤2,则假设2成立. |
| ||
| ||
| ||
| ||
| 实验步骤 | 预期现象和结论 |
| b | 褪色 |
| d | 变蓝色 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、①和③ | B、②和③ |
| C、③和④ | D、②和⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
- 2 |
- 2 |
- 3 |
- 2 |
- 3 |
- 3 |
- 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
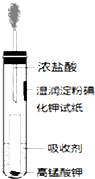 氯气是氯碱工业的主要产品之一,是一种常用的消毒剂,其消毒原理是与水反应生成了次氯酸:Cl2+H2O?HCl+HClO K=4.5×10-4
氯气是氯碱工业的主要产品之一,是一种常用的消毒剂,其消毒原理是与水反应生成了次氯酸:Cl2+H2O?HCl+HClO K=4.5×10-4查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将BaCl2溶液分别滴入两种液体中,变浑浊的是硫酸溶液 |
| B、将两种液体分别滴入碳酸氢钠粉末中,有气泡产生的是硫酸溶液 |
| C、将酚酞溶液分别滴入两种液体中,变红色的是硫酸溶液 |
| D、测试这两种液体的导电性,导电性强的是硫酸溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、5种 | B、6种 | C、9种 | D、10种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| NaOH的质量分数 | 阳极析出物质的质量/g | 阴极析出物质的质量/g | |
| A | 0.062(6.2%) | 19 | 152 |
| B | 0.062(6.2%) | 152 | 19 |
| C | 0.042(4.2%) | 1.2 | 9.4 |
| D | 0.042(4.2%) | 9.4 | 1.2 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com