
【题目】镍氢电池是二十世纪九十年代发展起来的一种新型绿色电池,具有高能量、长寿命、无污染等特点。用吸附了氢气的纳米碳管等材料制作的二次电池的原理如图1所示。电池的总反应式为:2Ni(OH)2 ![]() H2+2NiO(OH)
H2+2NiO(OH)

(1)①镍氢电池充电时,碳电极连接直流电源的______极。阳极的电极反应式为______
②镍氢电池放电时,OH-移向______(填“碳电极”或“镍电极”)。
(2)除了用纳米碳管等材料储氢外,还可使用有机物,如利用环己烷和苯之间的可逆反应来实现脱氢和加氢。一定条件下,利用图2装置可实现有机物的电化学储氢(忽略其它有机物)。
①A为电源的______极。
②电极E上产生的气体为______。
【答案】负 Ni(OH)2+OH--e-=NiO(OH)+H2O 碳电极 负极 氧气
【解析】
2Ni(OH)2 ![]() H2+2NiO(OH),在放电过程中,镍电极化合价降低,作正极,碳电极电极作负极。
H2+2NiO(OH),在放电过程中,镍电极化合价降低,作正极,碳电极电极作负极。
⑴①镍氢电池充电时,电池正极连接电源的正极,电池负极连接电源的负极,因此碳电极连接直流电源的负极,阳极是NiO(OH)转变为Ni(OH)2,即阳极的电极反应式为Ni(OH)2+OH--e-=NiO(OH)+H2O,故答案为:负;Ni(OH)2+OH--e-=NiO(OH)+H2O;
②镍氢电池放电时,根据“同性相吸”原则,则OH-移向碳电极,故答案为:碳电极;
⑵①左边是苯变为环己烷,化合价降低,作阴极,因此A为电源的负极,故答案为:负;
②电极E为阳极,阳极是氢氧根放电变为氧气,因此E上产生的气体为氧气,故答案为:氧气。


 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:
【题目】已知元素原子的下列结构或性质,能确定其在周期表中位置的是( )
A. 某元素原子的第二电子层电子排布图为![]()
B. 某元素在某种化合物中的化合价为+4
C. 某元素的原子最外层上电子数为6
D. 某元素的外围电子排布式为5s25p1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示对应化学反应的离子方程式正确的是
A.氯气溶于水:Cl2+H2O![]() H++Cl-+HClO
H++Cl-+HClO
B.MnO2与浓盐酸反应制Cl2:MnO2+4HCl![]() Mn2++2Cl-+Cl2↑+2H2O
Mn2++2Cl-+Cl2↑+2H2O
C.Na2O2溶于水产生O2:Na2O2+H2O=2Na++2OH-+O2↑
D.向NaHCO3溶液中加过量澄清石灰水:2HCO+Ca2++2OH-=CaCO3↓+CO![]() +2H2O
+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物甲、乙、丙是合成消炎药洛索洛芬的中间体。

下列说法正确的是
A.甲分子中所有碳原子一定处于同一平面
B.丙分子中含有1个手性碳原子
C.一定条件下,甲、乙、丙均能与H2发生加成反应
D.1 mol乙与足量NaOH溶液充分反应,最多消耗NaOH的物质的量为3 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在指定溶液中,能大量共存的是( )
![]() 无色溶液中:
无色溶液中:![]()
![]()
![]()
![]()
![]()
![]() 的溶液中:
的溶液中:![]()
![]()
![]()
![]()
![]()
![]() 水电离的
水电离的![]() 浓度为
浓度为![]() 的溶液中:
的溶液中:![]()
![]()
![]()
![]()
![]()
![]() 加入铝粉放出氢气的溶液中:
加入铝粉放出氢气的溶液中:![]()
![]()
![]()
![]()
![]()
![]()
![]() 使甲基橙变红的溶液中:
使甲基橙变红的溶液中:![]()
![]()
![]()
![]()
![]()
![]() 中性溶液中:
中性溶液中:![]()
![]()
![]()
![]()
![]() 能溶解铜粉的溶液:
能溶解铜粉的溶液:![]()
![]()
![]()
![]()
![]()
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国化学家研究的一种新型复合光催化剂[碳纳米点(CQDs)/氮化碳(C3N4)纳米复合物]可以利用太阳光实现高效分解水,其原理如图所示。下列说法正确的是
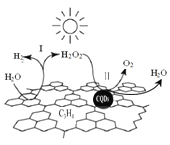
A. C3N4中C的化合价为 -4
B. 反应的两个阶段均为吸热过程
C. 阶段Ⅱ中,H2O2既是氧化剂,又是还原剂
D. 通过该反应,实现了化学能向太阳能的转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可利用环己醇的氧化反应制备环己酮,反应原理和实验装置(部分夹持装置略去)如下:
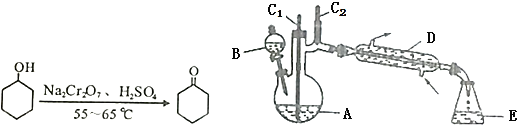
有关物质的物理性质见表。
物质 | 沸点(℃) | 密度(g/cm3,20℃) | 溶解性 |
环己醇 | 161.1(97.8)* | 0.96 | 能溶于水和醚 |
环己酮 | 155.6(95.0)* | 0.95 | 微溶于水,能溶于醚 |
水 | 100.0 | 1.0 |
*括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点。
实验中通过装置B将酸性Na2Cr2O7溶液加到盛有10mL环己醇的A中,在55~65℃进行反应。反应完成后,加入适量水,蒸馏,收集95~100℃的馏分,得到主要含环己酮粗品和水的混合物。
(1)仪器D的名称为_____。
(2)①滴加酸性Na2Cr2O7溶液时反应的离子方程式为______________;(![]() 被还原为Cr3+)
被还原为Cr3+)
②蒸馏不能分离环己酮和水的原因是_____。
(3)环己酮需要经过以下操作提纯:
a.往液体中加入NaCl固体至饱和,静置,分液
b.水层用乙醚(乙醚沸点34.6℃,易燃烧)萃取,萃取液并入有机层
c.加入无水MgSO4固体,除去有机物中少量的水
d.过滤
e.蒸馏、除去乙醚后,收集151~156℃馏分
①b中水层用乙醚萃取的目的是_____;
②上述操作a、d中使用的玻璃仪器除烧杯、玻璃棒外,还需要的玻璃仪器有____、___,操作a中,加入NaCl固体的作用是_____。
(4)恢复至室温时,分离得到纯产品体积为8mL,则环己酮的产率为____。(保留3位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于反应过程中的先后顺序,下列评价正确的是
A.向浓度都为0.1mol/L的FeCl3和CuCl2加入铁粉,溶质CuCl2首先与铁粉反应
B.向过量的Ba(OH)2溶液中滴加少量的KAl(SO4)2溶液,开始没有白色沉淀生成
C.向浓度都为0.1mol/L 的Na2CO3和NaOH的混合溶液通入CO2气体,NaOH首先反应
D.向浓度为0.1mol/L的FeCl3溶液中,加入质量相同、颗粒大小相同的铁和铜,铜单质首先参加反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com