
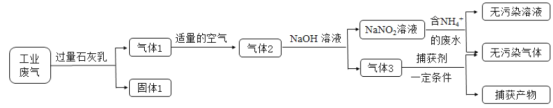
【题目】氮氧化合物和二氧化硫是引起雾霾的重要物质,工业用多种方法来治理。某种综合处理含NH4+废水和工业废气(主要含NO、CO、CO2、SO2、N2)的流程如图:
已知:NO+NO2+2NaOH=2NaNO2+H2O 2NO2+2NaOH=NaNO3+NaNO2+H2O
(1)固体1的主要成分有Ca(OH)2、__________(填化学式)。
(2)若实验室需要配制3 mol·L-1NaOH溶液1L进行模拟测试,需称取NaOH固体质量为__________g。
(3)用NaNO2溶液处理含NH4+废水反应的离子方程式为__________。
(4)验证废水中NH4+已基本除净的方法是___________(写出操作、现象与结论)。
(5)气体1转化为气体2时空气不能过量的原因是__________。
(6)捕获剂捕获的气体主要是__________(填化学式)。
(7)流程中生成的NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O;I2可以使淀粉变蓝。根据上述反应,选择生活中常见的物质和有关试剂进行实验,以鉴别NaNO2和NaCl。需选用的物质是__________(填序号)。
①水 ②淀粉碘化钾试纸 ③淀粉 ④白酒 ⑤白醋
A.①③⑤ B.①②④ C.①②⑤ D.①②③⑤
【答案】CaCO3 、CaSO3 120 NH4++NO2-=N2↑+2H2O 取少量处理后废水于试管中,加入NaOH溶液加热,将湿润的红色石蕊试纸放在试管口,若无明显现象则可证明NH4+已基本除净 气体1转化为气体2时,其中NO:NO2物质的量之比为1:1时才可以被NaOH溶液完全转化成NaNO2,若空气过量,则与NaOH反应生成NaNO3和NaNO2的混合溶液,因此空气不能过量 CO C
【解析】
工业废气(主要含NO、CO、CO2、SO2、N2)用过量石灰乳吸收,CO2、SO2与Ca(OH)2反应生成CaCO3、CaSO3,成为固体1的主要成分,此时气体1为NO、CO、N2;通入适量空气,主要与NO作用生成NO2,成为空气2的主要成分;通入NaOH溶液中,从产物NaNO2看,前面通入的空气,只能将一部分NO氧化为NO2,否则生成的NaNO2中会混入NaNO3;NO2-与NH4+发生氧化还原反应,生成N2和H2O,气体3为CO,被捕获剂捕获。
(1)从以上分析可知,固体1的主要成分有Ca(OH)2、CaCO3、CaSO3。答案为:CaCO3、CaSO3;
(2)若实验室需要配制3 mol·L-1 NaOH溶液1L进行模拟测试,需称取NaOH固体质量为3 mol·L-1 ×1L×40g/mol=120 g。答案为:120;
(3)用NaNO2溶液处理含NH4+废水时,NO2-与NH4+反应生成N2和H2O,反应的离子方程式为NH4++NO2-=N2↑+2H2O。答案为:NH4++NO2-=N2↑+2H2O;
(4)验证废水中NH4+已基本除净,可加碱检测气体的性质,方法是取少量处理后废水于试管中,加入NaOH溶液加热,将湿润的红色石蕊试纸放在试管口,若无明显现象则可证明NH4+已基本除净。答案为:取少量处理后废水于试管中,加入NaOH溶液加热,将湿润的红色石蕊试纸放在试管口,若无明显现象则可证明NH4+已基本除净;
(5)由以上分析知,气体1转化为气体2时空气不能过量的原因是气体1转化为气体2时,其中n(NO):n(NO2)物质的量之比为1:1时才可以被NaOH溶液完全转化成NaNO2,若空气过量,则与NaOH反应生成NaNO3和NaNO2的混合溶液,因此空气不能过量。答案为:气体1转化为气体2时,其中n(NO):n(NO2)物质的量之比为1:1时才可以被NaOH溶液完全转化成NaNO2,若空气过量,则与NaOH反应生成NaNO3和NaNO2的混合溶液,因此空气不能过量;
(6)由以上分析可知,捕获剂捕获的气体主要是CO。答案为:CO;
(7)鉴别NaNO2和NaCl,需利用反应2NaNO2+4HI=2NO↑+I2+2NaI+2H2O,所以需加I-、淀粉、酸,从而确定选用的物质是①②⑤,故选C。答案为:C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W原子序数依次增大。X氢化物的水溶性显碱性;Y在元素周期表中所处的周期序数与族序数相等;Z单质是将太阳能转化为电能的常用材料,也是一种半导体材料;W是重要的“成盐元素”,主要以钠盐的形式存在于海水中。请回答:
(1)Y在元素周期表中的位置是________。
(2)Y的最高氧化物相应水化物具有______(填“酸性”、“碱性”、“两性”)。并写出其电离方程式______。
(3)X氢化物的水溶液与W氢化物的水溶液混合后恰好反应时,溶液呈__性(填“酸”、“碱”或“中”),用离子方程式表示其原因是__。
(4)Z和W比较,非金属性较弱的是_______(填元素符号)。下列可以验证这一结论的是_______(填序号)。
a.元素在地壳中的含量
b.最高价氧化物对应水化物的酸性
c.氢化物的水溶性
d.Z与W以共价键形成化合物时,Z或W显示的化合价
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯催化氧化成乙醛可设计成如下图所示的燃料电池,能在制备乙醛的同时获得电能,其总反应为:2CH2=CH2+O2→2CH3CHO。下列有关说法正确的是
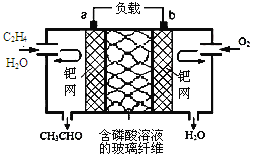
A.a电极发生还原反应
B.放电时,每转移2mol电子,理论上需要消耗28g乙烯
C.b极反应式为:O2+4e-+2H2O=4OH-
D.电子移动方向:电极a→磷酸溶液→电极b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)纯碱是一种重要的化工原料。目前制碱工业主要有“氨碱法”和“联合制碱法”两种工艺。
①“氨碱法”产生大量CaCl2废弃物,写出该工艺中产生CaCl2的化学方程式:___;
②CO2是制碱工业的重要原料,“联合制碱法”与“氨碱法”中CO2的来源有何不同?___;
(2)某探究活动小组根据上述制碱原理,进行碳酸氢钠的制备实验,同学们按各自设计的方案实验.①一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如图所示(图中夹持、固定用的仪器未画出)试回答下列有关问题:
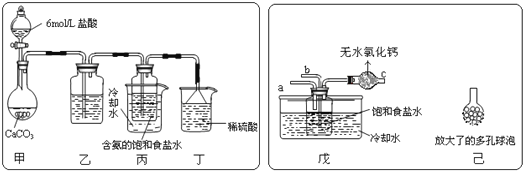
(Ⅰ)乙装置中的试剂是___;其作用是____;
(Ⅱ)丁装置中稀硫酸的作用是___;
(Ⅲ)实验结束后,分离出NaHCO3晶体的操作是___(填分离操作的名称).该操作所需是玻璃仪器有____。
②另一位同学用图中戊装置(其它装置未画出)进行实验。
(Ⅰ)实验时,须先从__(“a”或“b”)管通入___气体,说明原因___。
(Ⅱ)有同学建议在戊装置的b管下端连接己装置,理由是___。
(III)碳酸氢钠受热所得固体12.28g与足量石灰水充分反应,所得沉淀经洗涤、干燥质量为12.00g,则所得固体中碳酸钠的质量分数为:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氰基丙烯酸甲酯(G:![]() )的合成路线如下:
)的合成路线如下:
![]()
![]()
![]() ―→
―→![]() ―→
―→![]()
已知:①A的相对分子质量为58,氧元素质量分数为0.276,核磁共振氢谱显示为单峰
②![]()
![]()
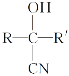
回答下列问题:
(1)A 的化学名称为________。
(2)B的结构简式为________,其核磁共振氢谱显示为________组峰,峰面积比为________。
(3)G中的官能团有________、________、________(填官能团名称)。
(4)G的同分异构体中,与G具有相同官能团且能发生银镜反应的共有________种(不含立体异构)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中进行的反应C(s)+H2O(g)![]() CO(g)+H2(g),能使反应速率加快的措施有( )
CO(g)+H2(g),能使反应速率加快的措施有( )
①增加炭的量②升高温度③将炭粉碎④恒容通入水蒸气⑤通过减小容器体积增大压强⑥恒容通入N2
A.②③④⑤B.②③④⑤⑥C.①②③④⑤D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯的产量通常用来衡量一个国家的石油化工水平,某化学实验小组为了探究石蜡油(17个碳以上的液态烷烃混合物)分解产物中有乙烯存在,设计了如下实验方案:
(查阅资料可知:乙烯与酸性高锰酸钾溶液反应产生二氧化碳。)
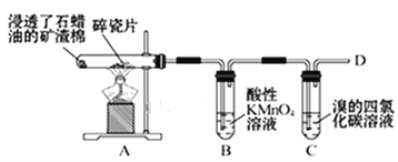
(1)乙烯的结构式是___。
(2)B中实验现象:___。
(3)C中发生反应的化学方程式:__,反应类型:___。
(4)通过上述实验探究可知,除去乙烷中混有的乙烯,可以选择的试剂是___。
A.水 B.溴水
C.氢氧化钠溶液 D.酸性高锰酸钾溶液
(5)关于乙烯,下列说法中不正确的是___。
A.聚乙烯塑料可以用做食品包装袋
B.乙烯在一定条件下可以和水反应制乙醇
C.乙烯分子中所有原子不共面
D.乙烯是一种植物生长调节剂,可以延长果实和花朵的成熟期
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列中心原子的杂化轨道类型和分子立体构型不正确的是( )
A. PCl3中P原子采用sp3杂化,为三角锥形
B. BCl3中B原子采用sp2杂化,为平面三角形
C. CS2中C原子采用sp杂化,为直线形
D. H2S中S原子采用sp杂化,为直线形
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增大。m、p、q、r、s是由这些元素组成的二元化合物,常温常压下r为液体,其余均为无色气体。m的摩尔质量为p的2倍,n是Y元素的单质,是绿色植物光合作用产生的无色气体,p物质能使湿润的红色石蕊试纸变蓝,q能使品红溶液褪色。上述物质的转化关系如图所示。下列说法正确的是( )

A. q与s均为酸性氧化物B. Z的含氧酸是一种强酸
C. X、Y分别与W形成10e-的微粒能反应生成一种气体D. 原子半径:W<Y<X
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com