
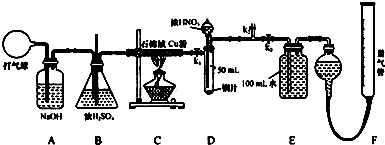
分析 (1)根据影响反应速率的因素分析,增大与氧气接触面积会使反应迅速;
(2)气球中的空气成分主要是氧气、氮气、二氧化碳、水蒸气等,通过氢氧化钠溶液除去二氧化碳,通过浓硫酸除去水蒸气;C装置是反应掉空气中的氧气;D装置是验证铜和浓硝酸反应中可能产生一氧化氮气体,必须保证不能含有氧气,才能在后续试验中通过测定气体体积判断一氧化氮气体的存在,所以D中充满氮气体积为50ml;按照气体流向进行开关的操作;
(3)若C装置的硬质玻璃管中出现堵塞,导致B中气体压强变大,则锥形瓶中玻璃管内液面上升;
(4)D中发生的反应一定是铜和浓硝酸的反应生成二氧化氮气体,同时可能硝酸变稀生成一氧化氮气体;加入四氯化碳的目的是把生成的气体全部排到E中吸收;
(5)根据装置的特点和压强关系进行分析判断.
解答 解:(1)将铜粉分散在石棉绒中可以增大铜粉与氧气的接触面积,加快反应速率使反应更充分,故答案为:增大铜粉与氧接触面积,使反应迅速、充分;
(2)气球中的空气成分主要是氧气、氮气、二氧化碳、水蒸气等,通过氢氧化钠溶液除去二氧化碳,通过浓硫酸除去水蒸气;C装置是反应掉空气中的氧气,所以进入D装置的气体主要是氮气,试管体积为50ml,进入的氮气体积为50ml,通入氮气目的是把试管中的空气排净,避免生成的一氧化氮气体被氧气氧化为二氧化氮,无法验证铜和浓硝酸反应产物中 有一氧化氮气体生成,依据气体流向,开关操作是关闭K3,打开K1、K2,让氮气把试管中的空气赶净,更好的利用后续试验测定气体体积和验证一氧化氮气体的生成,
故答案为:N2;排出D中的空气;K3 ;K1、K2;
(3)若C装置的硬质玻璃管中出现堵塞,导致B中气体压强变大,则锥形瓶中玻璃管内液面上升,故答案为:锥形瓶中玻璃管内液面上升;
(4)关闭K1、K2,打开K3,由分液漏斗向D中滴加浓硝酸,一定发生的反应是铜和浓硝酸反应生成硝酸铜二氧化氮和水,可能发生的反应是浓硝酸变稀后和铜的反应生成硝酸铜一氧化氮和水;D中一定发生反应的离子方程式:Cu+2NO3-+4H+=Cu2++2NO2↑+2H2O;通过分液漏斗向D中加入CCl4至满,因为氮气和氮氧化物不溶于四氯化碳,是为了把氮气和生成的气体全部排入到E装置吸收,故答案为:Cu+2NO3-+4H+=Cu2++2NO2↑+2H2O;
(5)DEF在关闭K3后装置是一套气密性完好的装置,若E中出现倒吸,可以调节F中量气管的液体高度改变压强,向下调节量气管,使E中的压强减少,防止液体进入E发生倒吸,或直接关闭K3,不让液体进入E装置,故答案为:向下调节量气管(或及时关闭K3).
点评 本题考查性质实验方案的设计,涉及硝酸的化学性质应用,量气管的正确使用方法,主要是分析装置中的气体流向和各装置的作用,装置图中的隐含条件气体体积的应用,酸碱反应的计算,题目较难,需要具备扎实的基础知识和实验基本操作技能.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | N4和N2互为同位素 | B. | 1个18O2中含有18个中子 | ||
| C. | 18O2 与16O2的性质完全相同 | D. | 2N5=5N2是化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | K与M、N均断开时,不发生任何化学反应 | |
| B. | K分别与M、N相连时,铜电极的质量都会增加 | |
| C. | K与N相连时,溶液中的Cl-向铜电极移动 | |
| D. | K与M相连时,Fe电极表面有铜析出 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 实验编号 | T/K | 反应时间/h | 反应物的物质的量配比n[CO(NH2)2]:n[MgCl2.6H2O] | 实验目的 |
| ① | 378 | 3 | 3:1 | (I)实验①和③探究反应物的物质的量配比对产率的影响 (II)实验②和④探究温度对产率的影响 (III)实验②和③探究反应时间对产率的影响 |
| ② | 378 | 4 | 4:1 | |
| ③ | 378 | 3 | ||
| ④ | 398 | 4 | 4:1 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 元素性质 | 元素编号 | |||||||
| A | B | C | D | E | F | G | H | |
| 氢化物的沸点(℃) | -60.7 | -33.4 | -111.5 | 100 | -87.7 | 19.54 | -84.9 | -161.5 |
| 最高化合价 | +6 | +5 | +4 | +5 | +7 | +4 | ||
最低化合价 | -2 | -3 | -4 | -2 | -3 | -1 | -1 | -4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2 | B. | N2O | C. | NO | D. | NO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 2-甲基-2,4-己二烯
2-甲基-2,4-己二烯 2,3-二甲基戊烷
2,3-二甲基戊烷查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com